Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{Cu}=\dfrac{80.80}{100}=64g\\ m_O=80-64=16g\\ n_{Cu}=\dfrac{64}{64}=1mol\\ n_O=\dfrac{16}{16}=1mol\\ CTHH:CuO\)

a) Với Fe3O4 thì Fe là 72,4% và O là 27,6%;
Với Fe2O3 thì Fe là 70% và O là 30%
b) Với SO2 thì S là 50% và O là 50%
Với SO3 thì S là 40% và O là 60%
c) mCu= \(\dfrac{80.80}{100}\)=64(g) ; mO=\(\dfrac{80.20}{100}\)=16(g)
nCu=\(\dfrac{64}{64}\)=1(mol) ; nO=\(\dfrac{16}{16}\)=1(mol)
Vậy CTHH của oxit đồng màu đen là: CuO
d) dA/H2=\(\dfrac{Ma}{2}\)=17 => MA=2.17=34(đvC)
H =\(\dfrac{5,88.34}{100}\)\(\approx\)2(đvC) ; S =\(\dfrac{94,12.34}{100}\)\(\approx\)32
=> CTHH của chất khí A là SH2

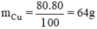
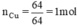 nguyên tử Cu.
nguyên tử Cu.
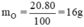
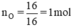 nguyên tử O.
nguyên tử O.
Suy ra trong 1 phân tử hợp chất có 1 nguyên tử Cu và 1 nguyên tử O.
Do đó công thức của oxit đồng màu đen là CuO.

Gọi công thức hoá học của hợp chất là: \(Cu_xS_yO_z\)
Ta có: \(64x:32y:16z=40:20:40\)
\(\Rightarrow x:y:z=\dfrac{40}{64}:\dfrac{20}{32}:\dfrac{40}{16}\)
\(\Rightarrow x:y:z=1:1:4\)
Vậy công thức hoá học đơn giản của hợp chất B là: \(\left(CuSO_4\right)n\)
Ta lại có: \(\left(CuSO_4\right)n=160\)
\(\Rightarrow160n=160\)
\(\Rightarrow n=1\)
Vậy công thức hoá học của hợp chất B là:\(CuSO_4\)

a) %Cl = 60,68%
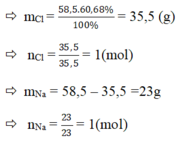
Vậy trong 1 phân tử hợp chất A có : 1 nguyên tử Na, 1 nguyên tử Cl.
⇒ CTHH của hợp chất A : NaCl
b)
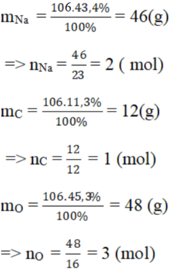
Vậy trong 1 phân tử hợp chất B có: 2 nguyên tử Na, 1 nguyên tử C, 3 nguyên tử O.
⇒ CTHH của hợp chất B : Na2CO3.

CuxOy
\(\frac{16y}{80}\) .100% = 20% => y= 1
=> 64x + 16= 80 => x= 1
=> công thức CuO
16y/80*100%=20% ta duoc y=1
64x+16=80 ta duoc x=1
vay cong thuc hoa hoc CuO

Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất là :
mCu = 80.80/100 = 64 (g)
mO = 80.20/100 = 16 (g)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất là :
nCu = 64/64 = 1 (mol)
nO = 16/16 = 1 (mol)
=> CTHH : CuO.
Gọi công thức hóa học của hợp chất A là CuxOy
Theo đề ra, ta có:
+ Khối lượng Cu: mCu = \(\frac{80.80}{100}=64\left(gam\right)\)
=> Số mol Cu: nCu = \(\frac{64}{64}=1\left(mol\right)\)
+ Khối lượng O: mO = 80 - 64 = 16 (gam)
=> Số mol O: nO = \(\frac{16}{16}=1\left(mol\right)\)
\(\Rightarrow\) x : y = 1 : 1
=> Công thức của A: CuO