Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có pthh:
\(Fe+S\underrightarrow{t^o}FeS\left(1\right)\)
x1 x1 x1 (mol)
Sau khi nung trong hỗn hợp A có :
\(\left(x-x_1\right)molS\)
\(\left(2x-x_1\right)molFe\)
và x1 mol FeS
- hòa tan A trong axit HCl dư :
\(Fe+2HCl\rightarrow FeCL_2+H_2\uparrow\left(2\right)\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\left(3\right)\)
Còn lại 0,4 g chất rắn B là lưu huỳnh dư
\(nS=x-x_1=\dfrac{0,4}{32}=0,0125\left(mol\right)\left(I\right)\)
Dung dịch C gồm HCl dư và FeCl2 với số mol là 2x .
Khí D gồm H2 và H2S .
Sục khí D từ từ vào dung dịch CuCl2 dư , chỉ có H2S phản ứng.
\(CuCl_2+H_2S\rightarrow CuS\downarrow+2HCl\left(4\right)\)
Kết tủa đen tạo thành là CuS
theo (1) (2) , (4) :
\(nCuS=x_1=\dfrac{4,8}{96}=0,05\left(mol\right)\left(II\right)\)
Kết hợp (I) ; và (II) ta có : x - x1= 0,0125
x = 0,0125 + 0,05 = 0,0625
Hiệu suất pứ tạo thành hh A:
Theo S: \(h\%=\dfrac{0,05}{0,0625}.100\%=80\%\)

Đáp án A
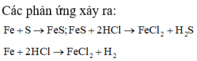
Hỗn hợp khí Z gồm H2S và H2. Đặt nFe=1mol . Dựa vào phương trình phản ứng ta thấy vì số mol khí sinh ra luôn là 1 mol với bất kì hiệu suất và tỉ lệ a:b nào nên:
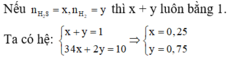
Theo đề bài hiệu suất phản ứng là 50% nhưng do chưa biết Fe hay S dư nên phải xét hai trường hợp. Tuy nhiên khi nhìn vào đáp án có thể thấy số mol sắt lớn hơn số mol lưu huỳnh nên hiệu suất được tính theo lưu huỳnh. Bảo toàn lưu huỳnh suy ra
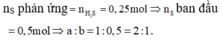

Đáp án A
Các phản ứng xảy ra:
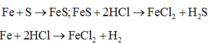
Hỗn hợp khí Z gồm H2S và H2. Đặt nFe=1mol . Dựa vào phương trình phản ứng ta thấy vì số mol khí sinh ra luôn là 1 mol với bất kì hiệu suất và tỉ lệ a:b nào nên:
Nếu ![]() thì x + y luôn bằng 1. Ta có hệ:
thì x + y luôn bằng 1. Ta có hệ:
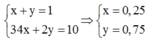
Theo đề bài hiệu suất phản ứng là 50% nhưng do chưa biết Fe hay S dư nên phải xét hai trường hợp. Tuy nhiên khi nhìn vào đáp án có thể thấy số mol sắt lớn hơn số mol lưu huỳnh nên hiệu suất được tính theo lưu huỳnh. Bảo toàn lưu huỳnh suy ra
nS phản ứng
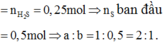

a) Hỗn hợp A gồm FeS (x mol), Fe dư (y mol) và S dư (0,8 gam)
FeS + 2HCl -------> FeCl2 + H2S
x………………..………x…….x (mol)
Fe + 2HCl -------> FeCl2 + H2
y…………………..…y……..y (mol)
=> Khí D gồm H2S và H2
\(M_D=\dfrac{34x+2y}{x+y}=9.2=18\) (*)
Khí D sục rất từ từ qua dung dịch CuCl2
H2S + CuCl2 -------> CuS + 2HCl
x………………………...x (mol)
=>\(n_{CuS}=x=\dfrac{9,6}{96}=0,1\left(mol\right)\)
Từ (*) => y = 0,1 (mol)
nFe = x+ y = 0,1 + 0,1= 0,2 (mol)
=> m = 0,2 .56 = 11,2 (g)
nS pư = x = 0,1 (mol)
=> p = 0,1.32 + 0,8 = 4 (g)
b) Dung dịch C chứa FeCl2
nFeCl2 = x + y = 0,2 (mol)
FeCl2 + 2NaOH -------> Fe(OH)2 + 2NaCl
0,2................................,.0,2 (mol)
4Fe(OH)2 + O2 + 2H2O -------> 4Fe(OH)3
0,2..............................................0,2 (mol)
2Fe(OH)3 ------> Fe2O3 + 3H2O
0,2........................0,1 (mol)
Chất rắn là Fe2O3
Theo PT => nFe2O3 = 0,1 mol
=> mFe2O3 = 0,1.160 = 16 gam

\(m_A=m_{S\left(dư\right)}=0,8\left(g\right)\)
\(\overline{M}_D=9.2=18\)
\(CuCl_2+H_2S\rightarrow CuS+2HCl\)
\(\Rightarrow n_{H2S}=n_{CuS\downarrow}=\frac{9,6}{96}=0,1\left(mol\right)\)
Gọi x là mol H2 trong D
\(\Rightarrow\frac{0,1.34+2x}{0,1+x}=18\)
\(\Leftrightarrow x=0,1\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe\left(dư\right)}=0,1\left(mol\right)\\n_{FeS}=0,1\left(mol\right)\end{matrix}\right.\)
\(Fe+S\rightarrow FeS\)
\(\Sigma n_{Fe}=0,1+0,1=0,2\left(mol\right)\)
\(\Rightarrow m_1=0,2.56=11,2\left(g\right)\)
\(\Rightarrow m_2=m_S=0,8+0,1.32=4\left(g\right)\)

- Chất rắn không tan trong HCL dư là S => m S dư = 3,8g
Kết tủa đen là CuS => n CuS = 0,1 = n H 2 S = nS phản ứng
m S phản ứng = 3,2g
0,2 mol Z gồm 0,1 mol H 2 S và 0,1 mol H 2
m ban đầu = 3,8 + 3,2 = 7g
Ta lại có
n Fe p / u = n S p / u = 0,1 mol
n Fe dư = n H 2 = 0,1 mol
n Fe ban đầu → m Fe ban đầu = 0,2 .56 = 1,12 g
Vậy m = 11,2 + 0,7 = 18,2 (gam)



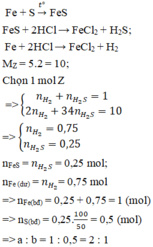
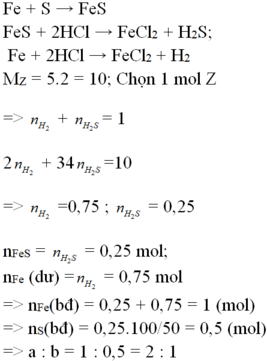
Câu 1:
\(PTHH:4R+xO_2\rightarrow2R_2O_x\)
\(n_{O2}=\frac{19,2}{32}=0,6\left(mol\right)\)
\(\Rightarrow n_R=\frac{4}{x}n_{O2}=\frac{2,4}{x}\left(mol\right)\)
BTKL:
\(m_R=m_{R2Ox}-m_{O2}\)
\(\Leftrightarrow40,8-19,2=21,6\)
\(\Rightarrow R=\frac{21,6}{\frac{2,4}{x}}=9x\left(\frac{g}{mol}\right)\)
Biện luận :
Nếu \(x=3\Rightarrow R=27\left(Al\right)\)
Vậy R là Al
Câu 2:
a,
Vì Hiệu suất phản ứng giữa Fe vs S không đạt 100%
=> Có Fe, S dư
Vì S không tác dụng với HCl
=> Chất rắn B là lưu huỳnh
\(n_{S\left(dư\right)}=\frac{0,4}{32}=0,0125\left(mol\right)\)
Bảo toàn nguyên tố "S"
\(n_{S\left(pư\right)}=n_{CuS}=\frac{4,8}{64+32}=0,05\left(mol\right)\)
\(n_{S\left(bđ\right)}=n_{S\left(pư\right)}+n_{S\left(dư\right)}\)
\(\Rightarrow n_{S\left(bđ\right)}=0,05+0,0125=0,0625\left(mol\right)\)
\(H=\frac{n_{S\left(pư\right)}}{n_{S\left(bđ\right)}}\)
\(\Rightarrow H=\frac{0,06}{0,0625}.100\%=80\%\)
b,
Ta có :
\(n_{S\left(bđ\right)}=0,0625\left(mol\right)\)
Mà \(n_{Fe}=2n_S\Rightarrow n_{Fe}=0,0625.2=0,125\left(mol\right)\)
\(n_{hh}=n_{Fe}+n_S\Leftrightarrow m_{hh}=0,125.56+0,0625.32=9\left(g\right)\)
Copy trên tuhoc365.
\n\nLink : https://tuhoc365.vn/qa/cho-m-gam-hon-hop-bot-fe-va-s-voi-ti-le-so-mol-sat-bang-2-lan-so-mol-luu-huynh-roi-dem-nung-khong-c/
\n