1. cho 19,2 lít O2 phản ứng hoàn toàn với kim loại R thu được 40,8g oxit. xác định R
2. cho m gam hỗn hợp bột Fe và S với tỉ lệ mol sắt bằng 2 lần số mol S rồi đem nung (ko có oxi), thu được hỗn hợp A. hòa tan A bằng dd HCl dư thu được 0,4g chất rắn B, dd C, khí C. sục khí D từ từ qua dd CuCl2 dư thấy tạo ra 4,8g kết tủa đen
a) tính hiệu suất phản ứng tạo thành hỗn hợp A (theo S)
b) tính m



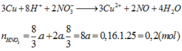
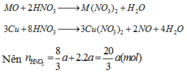
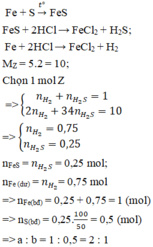
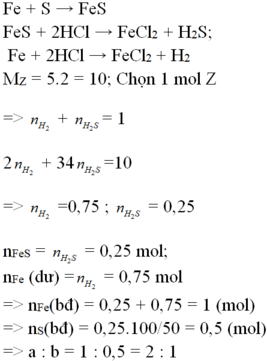
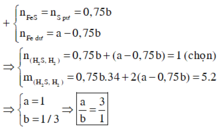
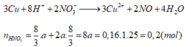
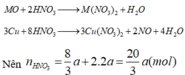
Câu 1:
\(PTHH:4R+xO_2\rightarrow2R_2O_x\)
\(n_{O2}=\frac{19,2}{32}=0,6\left(mol\right)\)
\(\Rightarrow n_R=\frac{4}{x}n_{O2}=\frac{2,4}{x}\left(mol\right)\)
BTKL:
\(m_R=m_{R2Ox}-m_{O2}\)
\(\Leftrightarrow40,8-19,2=21,6\)
\(\Rightarrow R=\frac{21,6}{\frac{2,4}{x}}=9x\left(\frac{g}{mol}\right)\)
Biện luận :
Nếu \(x=3\Rightarrow R=27\left(Al\right)\)
Vậy R là Al
Câu 2:
a,
Vì Hiệu suất phản ứng giữa Fe vs S không đạt 100%
=> Có Fe, S dư
Vì S không tác dụng với HCl
=> Chất rắn B là lưu huỳnh
\(n_{S\left(dư\right)}=\frac{0,4}{32}=0,0125\left(mol\right)\)
Bảo toàn nguyên tố "S"
\(n_{S\left(pư\right)}=n_{CuS}=\frac{4,8}{64+32}=0,05\left(mol\right)\)
\(n_{S\left(bđ\right)}=n_{S\left(pư\right)}+n_{S\left(dư\right)}\)
\(\Rightarrow n_{S\left(bđ\right)}=0,05+0,0125=0,0625\left(mol\right)\)
\(H=\frac{n_{S\left(pư\right)}}{n_{S\left(bđ\right)}}\)
\(\Rightarrow H=\frac{0,06}{0,0625}.100\%=80\%\)
b,
Ta có :
\(n_{S\left(bđ\right)}=0,0625\left(mol\right)\)
Mà \(n_{Fe}=2n_S\Rightarrow n_{Fe}=0,0625.2=0,125\left(mol\right)\)
\(n_{hh}=n_{Fe}+n_S\Leftrightarrow m_{hh}=0,125.56+0,0625.32=9\left(g\right)\)
Copy trên tuhoc365.
\n\nLink : https://tuhoc365.vn/qa/cho-m-gam-hon-hop-bot-fe-va-s-voi-ti-le-so-mol-sat-bang-2-lan-so-mol-luu-huynh-roi-dem-nung-khong-c/
\n