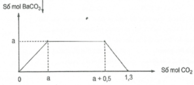
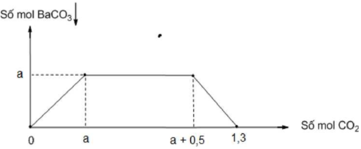
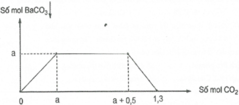
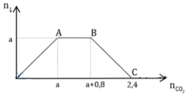
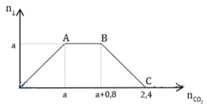
Dung dịch A chứa a mol Ca(OH)2. Hòa tan hết m gam NaOH vào dung dịch A, được dung dịch B. Sau đó, dẫn khí CO2 từ từ đến dư vào dung dịch B, ta thấy lượng kết tủa biến đổi theo đồ thị như hình vẽ bên. Xác định giá trị của a và m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

KOH + HCl → KCl + H2O
0,1........0,1.......0,1...................(mol)
Na2CO3 + HCl → NaHCO3 + NaCl
0,2.............0,2.............0,2............................(mol)
NaHCO3 + HCl → NaCl + CO2 + H2O
0,1.............0,1....................0,1..................(mol)
Suy ra : a = 0,2
Sau phản ứng : n NaHCO3 = 0,2 - 0,1 = 0,1(mol)
Bảo toàn nguyên tố C :
n CaCO3 = n NaHCO3 = 0,1(mol)
=> m = 0,1.100 = 10(gam)
anh ơi giải thích giúp e cái phương trình thứ hai được không ạ tại sao lại ra 0,2 ạ, trong khi đó số mol hcl dư là 0,4 - 0,1 =0,3

Đáp án B
Gọi số mol của Ba(OH)2 và NaOH lần lượt là a, b.
Nhận thấy tại 1,3 mol CO2 thì kết tủa bị hòa tan hoàn toàn
![]()
Tại (a + 0,5) mol CO2 thì kết tủa là a mol và lúc này xảy ra hiện tượng hòa tan kết tủa
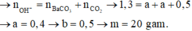


\(Ca\left(OH\right)_2+CO_2-->CaCO_3\downarrow+H_2O\left(1\right)\)
a___________a____________a
\(2NaOH+CO_2-->Na_2CO_3+H_2O\left(2\right)\)
\(\frac{m}{40}\)________\(\frac{m}{80}\) ________\(\frac{m}{80}\)
\(CaCO_3+H_2O+CO_2-->Ca\left(HCO_3\right)_2\left(4\right)\)
a________________a
\(Na_2CO_3+H_2O+CO_2-->2NaHCO_3\left(3\right)\)
\(\frac{m}{80}\) _______________\(\frac{m}{80}\)
=> theo sơ đồ : +Giai đoạn 1 : pt (1) kết tủa xuất hiện
+Giai đoạn 2: pt(2) , (3) kết tủa đến cực đại
+ Giai đoạn 3: pt (4) kết tủa tan dần đến hết
* Giai đoạn 2 có \(\Sigma_{mol}=a+0,5-a=0,5\left(mol\right)\)
⇔ \(\frac{m}{80}+\frac{m}{80}=0,5\Leftrightarrow\) \(\frac{2m}{80}=0,5\) ⇒ m=20(g)
Theo sơ đồ :
a+a+0,5=1,3=>2a=0,8=> a= 0,4(mol)