muốn thu 2,24l oxi thì dùng nguyên liệu nào tiết kiệm hơn KMnO4 hay MClO3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1) Làm giảm nhiệt độ nóng chảy của Al2O3.
2) Tiết kiệm được năng lượng, tạo được chất lỏng có tính dẫn điện tốt hơn Al2O3.
3) Tạo chất lỏng có tỉ khối nhỏ hơn nhôm, nổi lên bề mặt nhôm ngăn cản nhôm nóng chảy bị oxi hoá
Đáp án D

a)6KMnO4--->3K2MnO4 + 3MnO2 + 3O2 (1)
2KClO3---> 2KCl + 3O2 (2)
Dựa vào phương trình trên ---> thu cùng lượng O2, KMnO4 cần nhiều số mol hơn, và khối lượng nhiều hơn.
b)6KClO3-->6KCl + 9O2 (3)
1,3--->Cùng số mol, KClO3 cho nhiều O2 hơn.
c)Giả sử cả 2 chất cùng có khối lượng là 100g
nKMnO4=50/79(mol)
nKClO3=40/49
Thay vào các phương trình phản ứng tính ra mO2
Cụ thể: KMnO4 cho ra 800/79 (g) O2
KClO3 cho ra 1920/49 (g) O2
---> Cùng m thì KClO3 cho nhiều g O2 hơn.
d) Giả sử cần điều chế 32 g O2
--->nO2=1 mol
--->nKMnO4=2 mol--->mKMnO4=316g
và nKClO3=2/3 mol--->nKClO3=245/3g
Ta có:
-1000g KMnO4 <=> 200000đ
316 g=========>63200đ
-1000g KClO3 <=> 300000đ
245/3g========> 24500đ
Vậy để điều chế cùng lượng O2, KClO3 có giá thành rẻ hơn.

Giả sử cần điều chế 3,36lit O 2 tương đương với 0,15 mol O 2
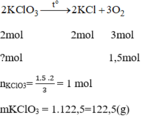
Số tiền mua 122,5g để điều chế 1,5mol O 2 :
0,1225.96000 = 11760 (đồng)
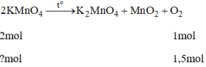
n K M n O 4 = 1,5 . 2 =3 mol
n K M n O 4 = 3.158 = 474 (g)
Số tiền mua 474g để điều chế 1,5 mol O 2 :
0,474.30000 = 14220(đồng)
Vậy để điều chế cùng 1 thể tích khí O 2 thì dùng K C l O 3 để điều chế kinh tế hơn mặc dù giá tiền cao mua 1 kg K C l O 3 cao hơn nhưng thể tích khí O 2 sinh ra nhiều hơn.

Chọn đáp án D.
Cả 3 ý đều là mục đích của việc dùng criolit, nên đọc kĩ để làm những

KClO3 --> KCl + O2
2KMnO4 --> MnO2 + O2 + K2MnO4
Để tạo 1 mol O2 cần 1 mol KClO3 nhưng cần 2 mol KMnO4
Vậy khi thu được lượng oxi như nhau thì cần dùng lượng KMnO4 nhiều hơn
Gọi n là số mol của 2 phản ứng
PTHH:
\(2KClO_3\xrightarrow[t^o]{MnO_2}2KCl+3O_2\left(1\right)\)
\(2KMnO_4\overset{t^o}{--->}K_2MnO_4+MnO_2+O_2\left(2\right)\)
Theo PT(1): \(n_{KClO_3}=\dfrac{2}{3}n\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=122,5.\dfrac{2}{3}n=\dfrac{245}{3}n\left(g\right)\)
Theo PT(2): \(n_{KMnO_4}=2n\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=158.2n=316n\left(g\right)\)
Ta thấy: \(\dfrac{245}{3}n< 316n\)
Vậy KMnO4 dùng nhiều hơn

Pt 2KMnO4\(\underrightarrow{t^o}\) K2MnO4+MnO2+O2 (1)
2KClO3 \(\underrightarrow{t^o}\) 2KCl +3O2 (2)
-Ta có nO2=\(\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
-Xét từng pt,
pt 1 : nKMnO4=2.nO2=0.2(mol) => mKMnO4=0,2.158=31.6(g)
pt2: nKClO3=\(\dfrac{2}{3}\).nO2=\(\dfrac{1}{15}\left(mol\right)\)=> mKClO3=\(\dfrac{1}{15}.122.5=8.16\left(g\right)\)
-So sánh 8.16<31.6=> dùng KClO3 tiết kiệm hơn