Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khi đốt mẫu gang trong oxi, cacbon cháy tạo thành C O 2 . Dẫn C O 2 qua nước vôi trong dư, toàn bộ lượng C O 2 chuyển thành kết tủa C a C O 3 .
C + O 2 → t ° C O 2 (1)
C O 2 + C a ( O H ) 2 → C a C O 3 ↑ + H 2 O (2)
Theo các phản ứng (1) và (2): n c = n C O 2 = n C a C O 3 = 0,01 (mol)
Khối lượng cacbon: m C = 0,01.12 = 0,12 (g)
Hàm lượng (%) cacbon trong mẫu gang:
%C = 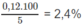

nMgSO4 = 0.2
CM MgSO4 = [Mg2+]=[SO42-]= 0.25M
Mg2 + 2OH- = Mg(OH)2
0.2-----0.4
=> V KOH = 0.8l
nBa(OH)2 = 0.2
=> CM Ba(OH)2 = 0.4 M
[Ba2+] = 0.4M
[OH-]= 2*0.4=0.8 M
H+ + OH - = H2O
0.4----0.4
=> nH2SO4 = 0.2 => V =1

a)
Do sau phản ứng có chứa nguyên tử Fe
=> A là muối cacbonat của Fe
CTHH: \(Fe_2\left(CO_3\right)_x\)
=> \(\frac{56.2}{56.2+60x}.100\%=48,28\%\) => x = 2
=> \(CTHH:FeCO_3\)
b)
Gọi số mol \(Fe_2O_3,Fe_3O_4\) là x,y (mol)
=> 160x + 232y = 39,2 (1)
\(n_{FeCO_3}=\frac{58}{116}0,5\left(mol\right)\)
Bảo toàn Fe => \(n_{Fe\left(FeCO_3\right)}=n_{Fe\left(Fe_2O_3\right)}+n_{Fe\left(Fe_3O_4\right)}\)
=> \(n_{FeCO_3}=2.n_{Fe_2O_3}+3.n_{Fe_3O_4}\)
=> \(2x+3y=0,5\) (2)
(1)(2) => \(\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
Gọi số mol \(NO_2\) thu được là a (mol)
Có: \(Fe_3^{+\frac{8}{3}}-1e\rightarrow3Fe^{+3}\)
____0,1----->0,1____________(mol)
\(NO_3^-+2H^++1e\rightarrow NO_2+H_2O\)
_______________a<-----a_____________(mol)
Áp dụng ĐLBT e => a = 0,1 (mol)
PTHH: \(4NO_2+O_2+2H_2O\rightarrow4HNO_3\)
_______0,07<--0,0175-------------->0,07________(mol)
=> \(n_{NO_2\left(dư\right)}=0,1-0,07=0,03\left(mol\right)\)
PTHH: \(3NO_2+H_2O\rightarrow2HNO_3+NO\uparrow\)
_______0,03------------------>0,02_____________(mol)
=> \(n_{HNO_3}=0,02+0,07=0,09\left(mol\right)\)
=> \(C_M\) dd \(HNO_3=\frac{0,09}{2}=0,045M\)


P b ( N O 3 ) + N a 2 S O 4 → P b S O 4 ↓ + 2 N a N O 3 A
tạo thành trong 500 ml = Số mol P b ( N O 3 ) trong 500 ml.
Lượng P b S O 4 hay P b 2 + có trong 1 lít nước :
3,168. 10 - 3 .2 = 6,336. 10 - 3 (mol).
Số gam chì có trong 1 lít:
6,336.10-3.207 = 1,312 (g/l) hay 1,312 mg/ml.
Vậy nước này bị nhiễm độc chì.