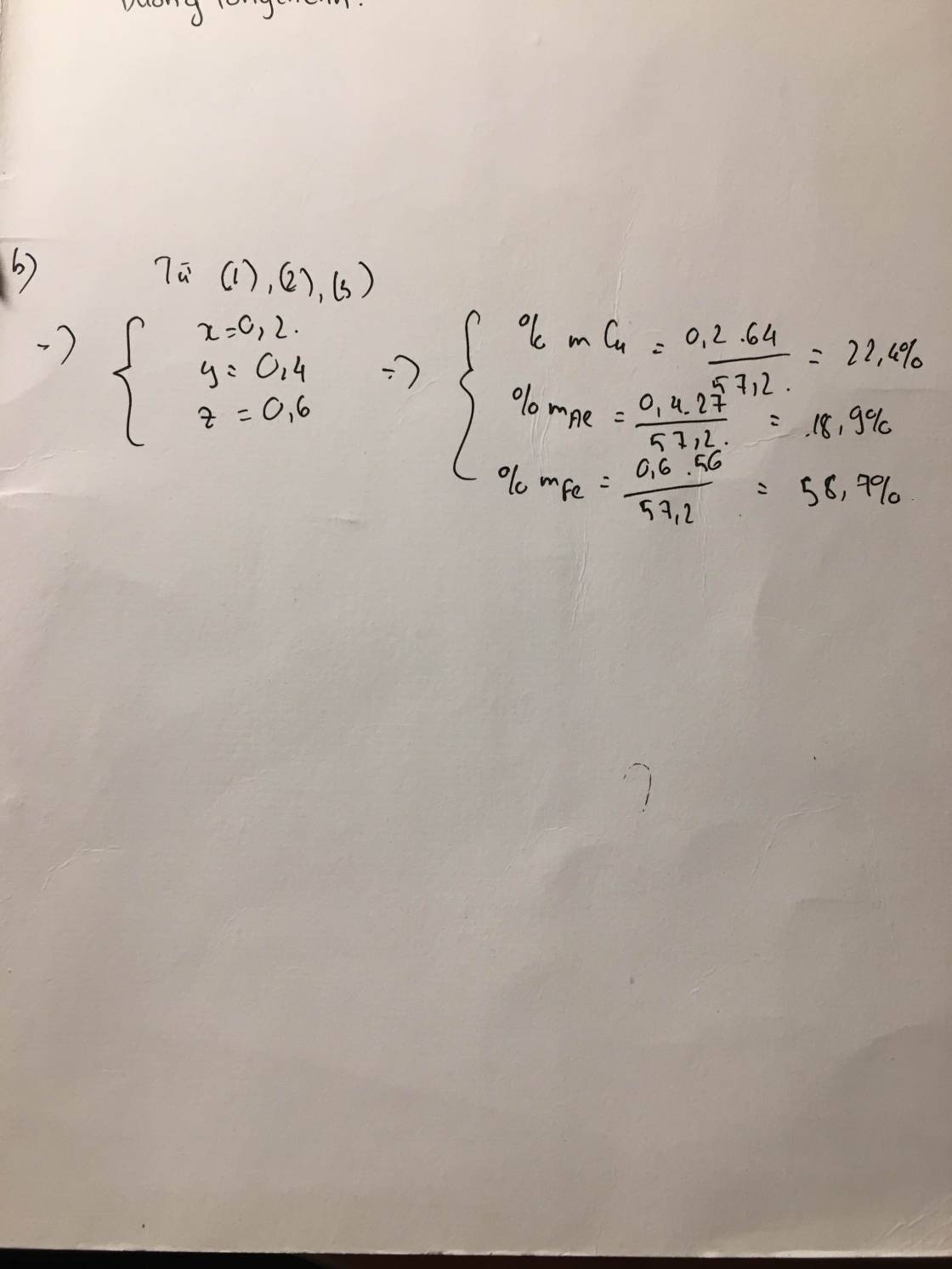Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

cho e hỏi chút tại sao : 1,2 mol X chứa k x mol Cu; ky mol Al và kz mol Fe vậy ạ

Gọi a,b,c lần lượt là số mol của Cu Fe Al
=> 64a + 56b + 27c = 57,2 (I)
PTHH
Fe + 2HCl ----> FeCl2 + H2
.b......2b..............b..........b..(mol)
2Al + 6HCl ----> 2AlCl3 + 3H2
..c.....3c................c..........1,5c
b+1,5c=26,8822,4=1,2b+1,5c=26,8822,4=1,2(II)
2Cu + O2 --to--> 2CuO
..a......0,5a
3Fe + 2O2 --to--> Fe3O4
..b....(2/3)b..
4Al + 3O2 --to--> 2Al2O3
c......0,75c....
=>0,5a+23b+0,75c=25,632=0,80,5a+23b+0,75c=25,632=0,8(III)
Từ (I) (II) và (III)
=>{a=0,2,b=0,6:c=0,4
Phần sau tự giải nhé

TN1: Gọi (nCu, nAl, nFe) = (a,b,c)
=> 64a + 27b + 56c = 14,3 (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
b----------------------->1,5b
Fe + 2HCl --> FeCl2 + H2
c----------------------->c
=> 1,5b + c = 0,3 (2)
TN2: Gọi (nCu, nAl, nFe) = (ak,bk,ck)
=> ak + bk + ck = 0,6 (3)
\(n_{O_2}=\dfrac{44,8}{22,4}.20\%=0,4\left(mol\right)\)
PTHH: 2Cu + O2 --to--> 2CuO
ak--->0,5ak
4Al + 3O2 --to--> 2Al2O3
bk--->0,75bk
3Fe + 2O2 --to--> Fe3O4
ck-->\(\dfrac{2}{3}ck\)
=> 0,5ak + 0,75bk + \(\dfrac{2}{3}ck\) = 0,4 (4)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,1\left(mol\right)\\c=0,15\left(mol\right)\\k=2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,05.64}{14,3}.100\%=22,38\%\\\%m_{Al}=\dfrac{0,1.27}{14,3}.100\%=18,88\%\\\%m_{Fe}=\dfrac{0,15.56}{14,3}.100\%=58,74\%\end{matrix}\right.\)

Giả sử 21,4 gam X chứa \(\left\{{}\begin{matrix}Cu:a\left(mol\right)\\Fe:2a\left(mol\right)\\R:b\left(mol\right)\end{matrix}\right.\)
=> 176a + b.MR = 21,4 (1)
\(n_{H_2}=\dfrac{15,68}{22,4}=0,7\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
2a--------------------->2a
2R + 2nHCl --> 2RCln + nH2
b---------------------->0,5bn
=> 2a + 0,5bn = 0,7 (2)
- 10,7g X chứa \(\left\{{}\begin{matrix}Cu:0,5a\left(mol\right)\\Fe:a\left(mol\right)\\R:0,5b\left(mol\right)\end{matrix}\right.\)
\(n_{Cl_2}=\dfrac{39,1-10,7}{71}=0,4\left(mol\right)\)
PTHH: Cu + Cl2 --to--> CuCl2
0,5a->0,5a
2Fe + 3Cl2 --to--> 2FeCl3
a-->1,5a
2R + nCl2 --to--> 2RCln
0,5b->0,25bn
=> 2a + 0,25bn = 0,4 (3)
(2)(3) => a = 0,05 (mol); bn = 1,2
=> \(\left\{{}\begin{matrix}n_{Cu}=0,05\left(mol\right)\\n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,05.64}{21,4}.100\%=14,95\%\\\%m_{Fe}=\dfrac{0,1.56}{21,4}.100\%=26,17\%\end{matrix}\right.\)

Gọi số mol Cu là x; Al là y và Fe là z
-> 64x+27y+56z=57,2
Cho 57,2 gam X tác dụng với HCl dư chỉ có Al và Fe phản ứng
Al + 3HCl -> AlCl3 +3/2 H2
Fe + 2HCl -> FeCl2 + H2
Ta có: nH2=26,88/22,4=1,2 mol =1,5y+z
1,2 mol X chứa k x mol Cu; ky mol Al và kz mol Fe
Cu + 1/2 O2 -> CuO
2Al +3/2 O2 -> Al2O3
2Fe + 3/2 O2 -> Fe2O3
Ta có: V O2=89,6.1/5=17,92 lít -> nO2=17,92/22,4=0,8 mol
-> nO2=0,5kx +0,75ky +0,75kz=0,8
-> (kx+ky+kz)/(0,5kx+0,75ky+0,75kz)=1,2/0,8=1,5
Giải được: x=317/730; y=242/365; z=15/73
-> mCu=27,79 gam; mAl=17,9 gam và mFe=11,51 gam

a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)

Bài 5:
mCu= 43,24% . 14,8\(\approx\) 6,4(g)
=>mFe\(\approx\) 14,8 - 6,4= 8,4(g)
=> nFe\(\approx\) 8,4/56\(\approx\) 0,15(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
nH2=nFe \(\approx\) 0,15 (mol)
=> V(H2,đktc) \(\approx\) 0,15 . 22,4\(\approx\) 3,36(l)
Bài 6:
nH2= 4,368/22,4=0,195(mol)
Đặt: nMg=a(mol); nAl=b(mol) (a,b>0)
PTHH: Mg + 2 HCl -> MgCl2 + H2
a________2a_____a_____a(mol)
2 Al + 6 HCl -> 2 AlCl3 +3 H2
b____3b____b______1,5b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}24a+27b=3,87\\a+1,5b=0,195\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,06\\b=0,09\end{matrix}\right.\)
a) nH2SO4= 2a+3b=0,39(mol)
=> mH2SO4= 0,39.98=38,22(g)
b) m(muối)= mMgSO4 + mAl2(SO4)3= 120a+ 133,5b= 120.0,06+133,5.0,09= 19,215(g)