Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi \(n_{H_2}=x\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{2}{3}x\) x ( mol )
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(x\) x ( mol )
\(a:b=\dfrac{\dfrac{2}{3}x.27}{65x}=\dfrac{18x}{65x}=\dfrac{18}{65}\)

2Al+6HCl-->2AlCl3+3H2 (1)
Zn+2HCl-->ZnCl2+H2 (2)
Gọi số mol của H2 ở 2 pt là a(mol)
Số mol của Al là:
nAl=2/3nH2=2/3.a(mol)
K/lượng của Al là:
m=n.M=2/3a.27=18a(g)
Số mol của Zn là:
nZn=nH2=a(mol)
K/lượng của Zn là:
m=n.M=a.65(g)
Tỉ lệ a,b là:
a/b=mAl/mZn=18a/65a=18/65
Vậy tỉ lệ a/b là 18/65

a)
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
2Al + 6HCl --> 2AlCl3 + 3H2
Fe + 2HCl --> FeCl2 + H2
b)\(n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\) => \(n_{H_2}=0,3\left(mol\right)\)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,2<---------------------------------------0,3
=> nAl = 0,2 (mol)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2---------------------->0,3
Fe + 2HCl --> FeCl2 + H2
0,1<---------------------0,1
=> a = 0,2.27 + 0,1.56 = 11(g)
\(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{11}.100\%=49,09\%\\\%m_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\end{matrix}\right.\)
ban oi cho hoi fe khong tac dung voi naoh ha mik thay tren internet co bao co ma

4) x,y lần lượt là số mol của M và M2O3
=> nOxi=3y=nCO2=0,3 => y=0,1
Đề cho x=y=0,1 =>0,1M+0,1(2M+48)=21,6 =>M=56 => Fe và Fe2O3
=> m=0,1.56 + 0,1.2.56=16,8
2)X + 2HCl === XCl2 + H2
n_h2 = 0,4 => X = 9,6/0,4 = 24 (Mg)
=>V_HCl = 0,4.2/1 = 0,8 l

Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
a, nH2 = nZn = 0,2 (mol)
⇒ VH2 = 0,2.24,79 = 4,958 (l)
b, nZnCl2 = nZn = 0,2 (mol)
⇒ mZnCl2 = 0,2.136 = 27,2 (g)
c, \(H=\dfrac{3,225}{4,958}.100\%\approx65,05\%\)

Theo gt ta có: $n_{Zn}=0,06(mol)$
$Zn+2HCl\rightarrow ZnCl_2+H_2$
a, Ta có: $n_{HCl}=0,12(mol)\Rightarrow m_{ddHCl}=30(g)$
b, Ta có: $n_{H_2}=0,06(mol)\Rightarrow V_{H_2}=1,344(l)$

Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
____0,2_____0,4_____0,2____0,2 (mol)
a, \(V_{H_2}=0,2.24,79=4,958\left(l\right)\)
b, mZnCl2 = 0,2.136 = 27,2 (g)
c, Đề cho VTT > VLT nên bạn xem lại đề nhé.

TN1: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Ta có: \(n_{Fe}=\dfrac{m_1}{56}\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=\dfrac{m_1}{56}\left(mol\right)\)
TN2: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Ta có: \(n_{Al}=\dfrac{m_2}{27}\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=\dfrac{m_2}{18}\left(mol\right)\)
Mà: \(V_2=1,5V_1\Rightarrow\dfrac{V_1}{V_2}=\dfrac{1}{1,5}=\dfrac{2}{3}\)
\(\Rightarrow\dfrac{n_1}{n_2}=\dfrac{n_{H_2\left(Fe\right)}}{n_{H_2\left(Al\right)}}=\dfrac{2}{3}\) \(\Rightarrow\dfrac{\dfrac{m_1}{56}}{\dfrac{m_2}{18}}=\dfrac{2}{3}\)
\(\Rightarrow\dfrac{m_1}{m_2}=\dfrac{56}{27}\)
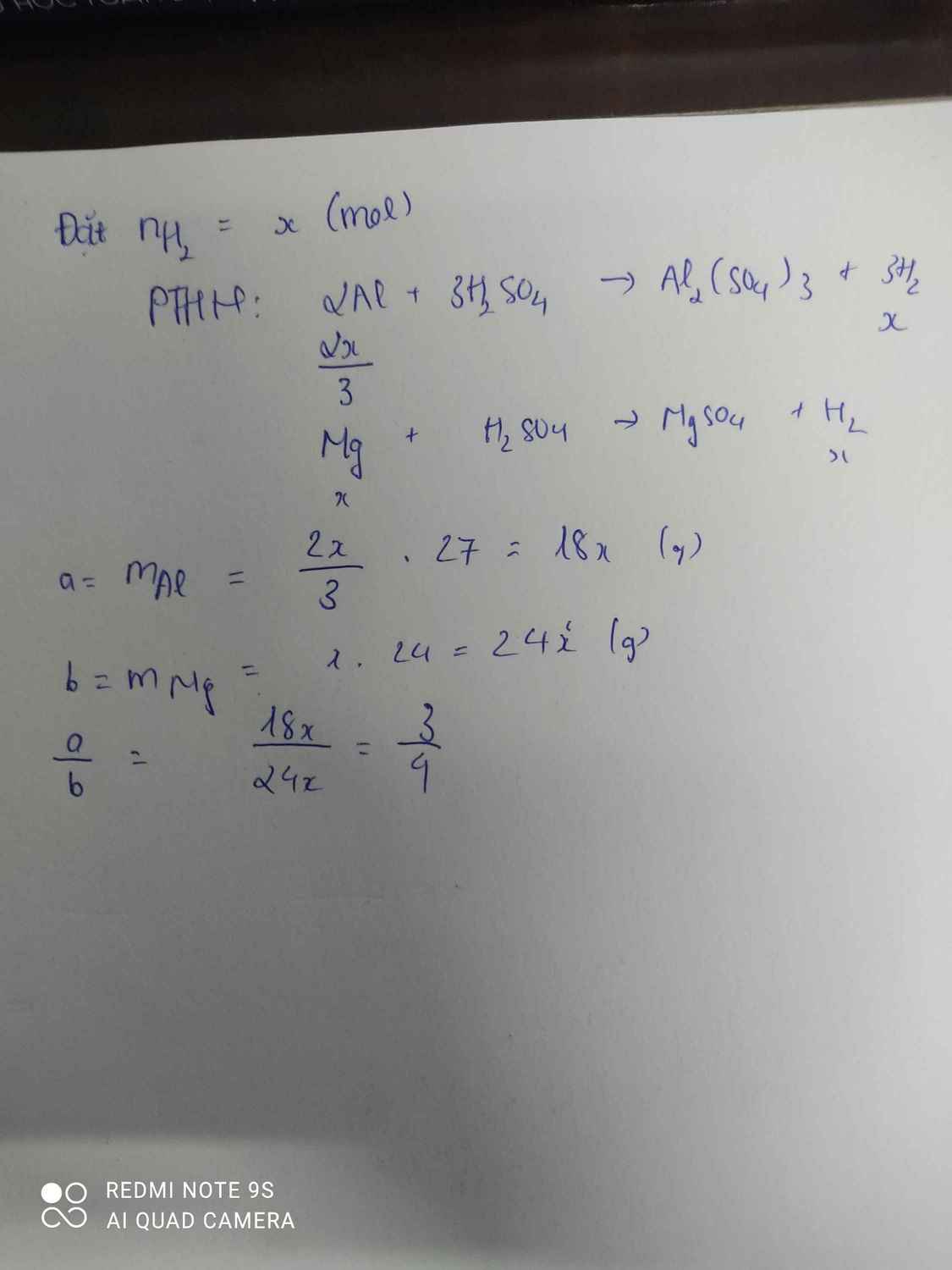
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Zn + 2HCl \to ZnCl_2 + H_2$
$n_{Al} = \dfrac{a}{27} (mol) \Rightarrow n_{H_2} = \dfrac{3}{2}n_{Al} = \dfrac{a}{18}(mol)$
$n_{Zn} = \dfrac{b}{65}(mol) \Rightarrow n_{H_2} = n_{Zn} = \dfrac{b}{65}(mol)$
$\Rightarrow \dfrac{a}{18} = \dfrac{b}{65}$
$\Rightarrow \dfrac{a}{b} = \dfrac{18}{65}$