

![]()
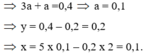
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


![]()
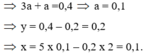

Chọn đáp án A
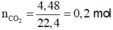
100 ml X + Ba(OH)2 dư → 0,2 mol BaCO3 ↓
![]()
100 ml X + HCl:
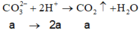
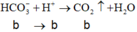
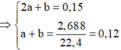
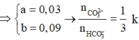
Trong 200 ml
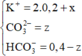
![]()
⇒ n C O 3 2 - = 0 , 1 m o l ; n H C O 3 - = 0 , 3 m o l
→ B T N T x = 0 , 1 . 2 + 0 , 3 - 0 , 2 . 2 = 0 , 1

Đáp án B
► Xét TN1: đặt nCO32– phản ứng = a; nHCO3– phản ứng = b.
⇒ nCO2 = a + b = 0,15 mol; nHCl phản ứng = 2a + b = 0,1875 mol
||⇒ giải hệ có: a = 0,0375 mol; b = 0,1125 mol ⇒ nCO32–/X : nHCO3–/X = a : b = 1 : 3.
► Xét TN2: ∑nC/X = n↓ = 0,25 mol ⇒ 250 ml X chứa 0,5 mol C.
Bảo toàn nguyên tố Cacbon: y = 0,5 – 0,25 = 0,25 mol.
● Chia 0,5 mol C thành 0,125 mol CO32– và 0,375 mol HCO3–.
Bảo toàn điện tích: nK+ = 0,625 mol. Bảo toàn nguyên tố Kali:
x = 0,625 – 0,25 × 2 = 0,125 mol

Đáp án B
n C O 2 = 0 , 2 m o l
Cho 100 ml dung dịch X vào dung dịch chứa 0,15 mol HCl thu được 0,12 mol CO2.
Do n C O 2 < n H C l < 2 n C O 2 nên dung dịch X chứa K2CO3 và KHCO3.
Gọi số mol K2CO3 và KHCO3 phản ứng lần lượt là a, b.
=> a+b= 0,12; 2a+b=0,15
Giải được a=0,03; b=0,09 vậy trong X tỉ lệ số mol K2CO3 và KHCO3 là 1:3.
Gọi số mol K2CO3 trong X là m suy ra KHCO3 là 3m.
Cho 100 ml dung dịch X tác dụng với Ba(OH)2 dư thu được 0,2 mol kết tủa BaCO3.
Do vậy 200 ml dung dịch X tác dụng thì thu được 0,4 mol kết tủa.
=> m+3m= 0,4=> m=0,1
Bảo toàn C: n K 2 C O 3 = 0 , 4 - 0 , 2 = 0 , 2
Bảo toàn K: n K O H = 0 , 1 . 2 + 0 , 3 - 0 , 2 . 2 = 0 , 1
Vậy x= 0,1