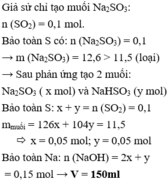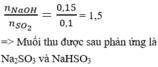Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1
\(n_{H2S}=\frac{8,96}{22,4}=0,4\left(mol\right)\)
\(m_{dd_{NaOH}}=1,28.500=640\left(g\right)\)
\(\Rightarrow n_{NaOH}=\frac{640.25\%}{40}=4\left(mol\right)\)
\(2NaOH+H_2S\rightarrow Na_2S+2H_2O\)
0,8_______0,4______0,4____________
Dư NaOH nên chỉ tạo Na2S
\(\Rightarrow C\%_{Na2S}=\frac{0,4.78.100}{0,4.34+640}=4,77\%\)
Câu 2 :
\(n_{H2S}=0,3\left(mol\right)\)
\(RS+H_2SO_4\rightarrow RSO_4+H_2S\)
0,3____0,3______________0,3
\(\Rightarrow m_{H2SO4}=29,4\left(g\right)\)
\(R+S\underrightarrow{^{to}}RS\)
0,3_____0,3
\(\Rightarrow M_R=\frac{16,8}{0,3}=56\left(Fe\right)\)
Câu 3 :
\(n_{Fe}=0,1\left(mol\right);n_S=0,05\left(mol\right)\)
\(PTHH:Fe+S\rightarrow FeS\)
Ban đầu :__0,1_0,05
Phứng_0,05__0,05
Sau___ 0,05 ___0 ____ 0,05
Nên Fe dư
\(n_{H2S}=n_{FeS}=0,05\left(mol\right)\)
\(2n_{Fe}=2n_{H2}\Rightarrow n_{H2}=0,05\left(mol\right)\)
\(V\%_{H2S}=n\%_{H2S}=\frac{0,05}{0,1}.100\%=50\%\)
\(V\%_{H2}=100\%-50\%=50\%\)
\(n_{HCl\left(pư\right)}=2n_{H2S}+2n_{H2}=0,05.2+0,05.2=2\)
Đổi :
500ml=0,5l
125ml=0,125l
\(n_{NaOH}=0,125.0,1=0,0125\left(mol\right)\)
\(n_{NaOH}=n_{NaCl}=n_{HCl\left(dư\right)}=0,0125\left(mol\right)\)
\(\Sigma n_{HCl\left(bđ\right)}=0,0125+2=2,0125\left(mol\right)\)
\(\Rightarrow CM_{HCl}=\frac{2,0125}{0,5}=4,025M\)
Câu 4 dài ( Mình chưa ngắn ra cho dễ nhìn nha )
a, \(n_{SO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
Đổi 800ml = 8l
\(n_{NaOH}=0,8.1=0,8\left(mol\right)\)
\(\frac{n_{NaOH}}{n_{SO2}}=\frac{0,8}{0,1}=8\)
Sinh ra muối Na2SO3, tính theo mol SO2
\(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
0,2________0,1_______0,1_____________
\(CM_{Na2SO3}=\frac{0,1}{0,8}=0,125M\)
\(CM_{NaOH\left(dư\right)}=\frac{0,8-0,2}{0,8}=0,75M\)
b,\(n_{SO2}=0,2\left(mol\right)\)
Đổi 250ml=0,25l
\(n_{NaOH}=0,25\left(mol\right)\)
\(\frac{n_{NaOH}}{n_{SO2}}=\frac{0,25}{0,2}=1,25\)
Sinh ra 2 muối NaHSO3 và Na2SO3
\(n_{NaHSO3}+n_{Na2SO3}=0,2\)
\(n_{NaHSO3}+2n_{Na2SO3}=0,25\)
\(\Rightarrow\left\{{}\begin{matrix}n_{NaHSO3}=0,15\\n_{Na2SO3}=0,05\end{matrix}\right.\)
\(m_{muoi}=m_{NaHSO3}+m_{Na2SO3}\Leftrightarrow m_{muoi}=0,15.104+0,05.126\)
\(\Rightarrow m_{muoi}=21,9\left(g\right)\)
c,\(n_{SO3}=0,03\left(mol\right)\)
\(n_{KOH}=\frac{13,95.1,147.28\%}{56}=0,08\)
\(\frac{m_{KOH}}{n_{SO2}}=\frac{0,08}{0,03}=2,67\)
Sinh ra muối K2SO3 và KOH dư
\(2KOH+SO_2\rightarrow K_2SO_3+H_2O\)
0,06_____0,03______0,03________
\(C\%_{KOH\left(Dư\right)}=\frac{\left(0,08-0,06\right).56}{13,95.1,147+0,03.64}.100\%=6,25\%\)
\(C\%_{K2SO3}=\frac{0,03.158}{13,95.1,147+0,03.64}.100\%=26,45\%\)

1.
n BaSO4 = 2,33 : 233 = 0,01 mol
=> n SO2 = 0,01 mol
=> V SO2 = 0,224 mol
2
nSO2 = 4,48 / 22,4 = 0,2 (mol)
nNaOH = 0,3.1= 0,3 (mol)
Đặt T = nNaOH / nSO2 = 0,3 / 0,2 = 1,5
Vì 1 < T < 1,5 nên sẽ tạo ra 2 phương trình :
Gọi x là số mol của SO2 (I)
y là số mol của SO2 (II)
SO2 + 2NaOH --> Na2SO3 + H2O
x 2x x
SO2 + NaOH --> NaHSO3
y y y
Ta có : x + y = 0,2 (1)
Mặt khác : 2x + y = 0,3 (2)
Từ (1) và (2) ta có hpt :
x + y = 0,2 <=> x = 0,1
2x + y = 0,3 y = 0,1
mNa2SO3 = 0,1.126 = 12,6 (g)
mNaHSO3 = 0,1.104 = 10,4 (g)
=> mmuối = 12,6 + 10,4 = 23 (g)
3
n SO2 = 0,1 mol
Giả sử phản ứng tạo 1 muối NaHSO3
BTNT S: nNaHSO3 = nSO2 = 0,1
=> m muối = 10,4 gam < 11,5 gam
Giả sử phản ứng tạo 1 muối Na2SO3
BTNT S: nNa2SO3 = nSO2 = 0,1 => m muối = 12,6 gam > 11,5 gam
Chứng tỏ phản ứng tạo hỗn hợp 2 muối NaHSO3 (a mol) và Na2SO3 (b mol)
Ta có hpt:
{a+b=0,1104
a+126b=11,5=>{a=0,05,b=0,05
BTNT Na => n NaOH = 2n Na2SO3 + n NaHSO3 = 0,15 mol
VNaOH = 0,15 :1 = 0,15 lít = 150ml

nSO2=0,1(mol)
nKOH=0,1(mol)
nKOH/nSO2=1/1
=> P.ứ tạo duy nhất muối axit
a) PTHH: SO2 + KOH -> KHSO3
b) nKHSO3=nKOH=0,1(mol)
=>mKHSO3= 120.0,1=12(g)
Chúc em học tốt!
Ta có: \(\left\{{}\begin{matrix}n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\n_{KOH}=0,1\cdot1=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\)Tạo muối axit
PTHH: \(SO_2+KOH\rightarrow KHSO_3\)
Theo PTHH: \(n_{KHSO_3}=0,1\left(mol\right)\) \(\Rightarrow m_{KHSO_3}=0,1\cdot136=13,6\left(g\right)\)

1/ nNaOH = 0.2 x 2 = 0.4 (mol)
nH2S = V/22.4 = 8.96/22.4 = 0.4 (mol)
NaOH/H2S = 1/1
NaOH + H2S => NaHS + H2O
Sản phẩm thu được: NaHS
VSO2 = 6.72 (l) => nSO2 = 0.3 (mol)
nNaOH = 0.5 x 0.9 = 0.45 (mol)
NaOH/SO2 = 1.5 => 2 muối
NaOH + SO2 => NaHSO3
2NaOH + SO2 => Na2SO3 + H2O
Gọi x,y lần lượt là số mol NaHSO3, Na2SO3
Ta có:
x + y = 0.3, x + 2y = 0.45
Giải phương trình => tính x,y rồi tính khối lượng 2 muối
Tính số mol của NaOH: n= CM.V= 0,2.2=0,4(mol); Số mol H2S= 8,96/22,4=0,4. Áp dụng Ba trên Mẹ dưới: nNaOH/ nH2S= 0,4/0,4=1 . Tỉ lệ 1 nên nó là muối axit hi Nên ra sp là NaHS và H2O
😀 😉

Ta có:
\(n_{SO2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{NaOH}=1.0,3=0,3\left(mol\right)\)
\(\frac{n_{NaOH}}{n_{SO2}}=\frac{0,3}{0,25}=1,2\)
Phản ứng tạo 2 muối
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
a_______2a _______ a_______
\(SO_2+NaOH\rightarrow NaHSO_3\)
b_______b__________b
Giải hệ PT:
\(\left\{{}\begin{matrix}a+b=0,25\\2a+b=0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Na2SO3}=0,05.126=6,3\left(g\right)\)
\(\Rightarrow m_{NaHSO3}=0,2.104=20,8\left(g\right)\)
\(\Rightarrow\Sigma m=20,8+6,3=27,1\left(g\right)\)
Đáp án đúng : A

Vì bài cho hỗn hợp bazơ mà chúng có tính chất tương tự nhau nên chúng ta gộp chung 2 bazơ để cho đơn giản hơn. Với 2 khí Cl2 và Br2 thì khí Cl2 có tính oxi hóa mạnh hơn sẽ tham gia phản ứng trước
Gọi CT chung kiềm là ROH.
\(PTHH:Cl_2+2ROH\rightarrow RCl+RClO+H_2O\)
Ta có:
\(\frac{n_{Cl2}}{1}< \frac{n_{ROH}}{2}\)
Nên Cl2 hết, ta tính khối lượng muối clorua theo Cl2
Giả sử muối chỉ có NaCl
\(\Rightarrow m=0,1.58,5=5,85\left(g\right)\)
Giả sử muối chỉ có KCl
\(\Rightarrow m=0,1.74,5=7,45\left(g\right)\)
Vậy khối lượng muối clorua thu được sau phản ứng nằm trong khoảng: (5,85; 7,45)g