Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi nMg = nAl = a (mol)
=> 24a + 27a = m
=> 51a = m
PTHH: 2Mg + O2 --to--> 2MgO
a---------------->a
4Al + 3O2 --to--> 2Al2O3
a------------------>0,5a
=> 40a + 51a = m + 2
=> 91a = 51a + 2
=> a = 0,05 (mol)
m = 0,05.24 + 0,05.27 = 2,55 (g)
Các PTHH của phản ứng:
2Mg+O2-->(to) MgO(1)
2mol 1mol 1mol
x mol 0,5mol
4Al+3O2-->(to) 2Al2O3 (2)
4mol 3mol 2mol
xmol 3/4mol
Khối lượng tăng bằng khối lượng của oxi tham gia phản ứng ⇒ mO2 = 2g.
nO2=2/32=0,625(mol)
Vì Mg và Al có số mol bằng nhau. Gọi nMg=nAl = x mol
Từ phương trình (1) và (2) ta có: nO2=0,5x+3/4x=0,625(mol)
=> x= 0,05(mol)
mhh=0,05(27+24) =2,55(g)

Các PTHH của phản ứng:
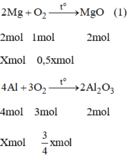
Khối lượng tăng bằng khối lượng của oxi tham gia phản ứng ⇒ m O 2 = 2g.
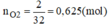
Vì Mg và Al có số mol bằng nhau. Gọi n M g = n A l = x mol
Từ phương trình (1) và (2) ta có:
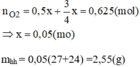

Ta có :
$m_{O_2\ pư} = m_{tăng} = 4(gam) \Rightarrow n_{O_2} = \dfrac{4}{32} = 0,125(mol)$
Gọi $n_{Mg} = n_{Al} = a(mol)$
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
Theo PTHH : $n_{O_2} = 0,5a + 0,75a = 0,125 \Rightarrow a = 0,1(mol)$
$\Rightarrow m = 0,1.24 + 0,1.27 = 5,1(gam)$

2Zn+O2--->2ZnO
x-------------------x
4Al+3O2--->2Al2O3
y----------------0,5y
Chất rắn tăng so với ban đầu 8g có nghĩa là
81x+51y-65x-27y=8
-->16x+24y=8(1)
Mặt khác: số mol 2 KL bằng nhau
--> x=y<=> x-y=0(2)
Từ 1 và 2 ta có hpt
\(\left\{{}\begin{matrix}16x+24y=8\\x-y=0\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,2\end{matrix}\right.\)
m =0,2(65+27)=18,4(g)
\(Zn+\frac{1}{2}O_2\rightarrow ZnO\)
x___ 1/2x__________
\(2Al+\frac{3}{2}O_2\rightarrow Al_2O_3\)
y___3/2y________
m tăng do có thêm khối lượng oxi
\(\rightarrow m_{tang}=m_{O2}=8\)
\(\rightarrow n_{O2}=\frac{8}{32}=0,35\left(mol\right)\)
\(x-y=0\)
\(\frac{1}{2}x+\frac{3}{2}y=0,125\)
\(\rightarrow x=y=0,125\)
\(m_{hh}=m_{Al}+m_{Zn}=0,125.27+0,125.65=11,5\left(g\right)\)

2Mg+O2--->2MgO
x_____1/2x
4Al+3O2--->2Al2O3
x___3/4x
Khối lượng tăng=mO2 p/ứ
nO2=2/32=0,0625(mol)
=>1/2x+3/4x=0,0625
=>x=0,05
=>a=0,05.24+0,05.27=2,55(g)

\(n_{H_2} = \dfrac{15,6-14}{2} = 0,8(mol)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Mg + 2HCl \to MgCl_2 + H_2\)
Gọi \(n_{Al} = a \ mol;n_{Mg} = b\ mol\)
Ta có :
\(\left\{{}\begin{matrix}27a+24b=15,6\\1,5a+b=0,8\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,4\\b=0,2\end{matrix}\right.\)
Vậy :
\(\%m_{Al} = \dfrac{0,4.27}{15,6}.100\% = 69,23\%\\ \%m_{Mg} = 100\% - 69,23\% = 30,77\%\)

nH2= \(\dfrac{0,896}{22,4}\) = 0,04(mol)
Mg + 2HCl \(\rightarrow\) MgCl2 + H2\(\uparrow\)
a \(\rightarrow\) a (mol)
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2\(\uparrow\) (ai dạy Al hóa trị II thế =.=)
b \(\rightarrow\) 1,5b (mol)
Gọi a,b lần lượt là số mol của Mg và Al
Theo đầu bài, ta có: \(\left\{{}\begin{matrix}24a+27b=0.78\\a+1,5b=0,04\end{matrix}\right.\) \(\Rightarrow\)\(\left\{{}\begin{matrix}a=0,01\\b=0,02\end{matrix}\right.\)
=> mMg= 0,01.24 = 0,24(g)
=> mAl = 0,78 - 0,24 = 0,54(g)