Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giả sử có 1 mol \(H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{2}{3}\) 1 1 ( mol )
\(m_{Al}=\dfrac{2}{3}.27=18g\)
\(m_{H_2SO_4}=1.98=98g\)
\(a:b=\dfrac{18}{98}=\dfrac{9}{49}\)

Giả sự đều sinh ra 1 mol H2
2Al+3H2SO4--->Al2(SO4)3+3H2
2/3_______________________1
=>a=2/3.27=18
Zn+H2SO4--->ZnSO4+H2
1___________________1
=>b=65
===> a/b=18/65

Gọi \(n_{H_2}=x\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{2}{3}x\) x ( mol )
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(x\) x ( mol )
\(a:b=\dfrac{\dfrac{2}{3}x.27}{65x}=\dfrac{18x}{65x}=\dfrac{18}{65}\)

2Al+ 3H2SO4-> Al2(SO4)3 +3H2
2a 3a Zn+H2SO4 -> ZnSO4 +H2 b b Theo bài ra ta có b=3a => a:b= 1:3
Cô sẽ chữa bài này như sau:
2Al+ 3H2SO4-> Al2(SO4)3 +3H2
a/27 ------------------------------a/18 Zn+H2SO4 -> ZnSO4 +H2 b/65 ----------------------b/65 a/18=b/65 <=> a=18b/65
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Zn + 2HCl \to ZnCl_2 + H_2$
$n_{Al} = \dfrac{a}{27} (mol) \Rightarrow n_{H_2} = \dfrac{3}{2}n_{Al} = \dfrac{a}{18}(mol)$
$n_{Zn} = \dfrac{b}{65}(mol) \Rightarrow n_{H_2} = n_{Zn} = \dfrac{b}{65}(mol)$
$\Rightarrow \dfrac{a}{18} = \dfrac{b}{65}$
$\Rightarrow \dfrac{a}{b} = \dfrac{18}{65}$

mFe=3,36 g; mAl=2,7 g; mAg=4,32 g
Giải thích các bước giải:
Gọi số mol Fe, Al, Ag trong mỗi phần là x, y, z.
P1: có Fe, Al phản ứng
nH2=0,105 mol; nSO2=0,13 mol
PTHH:
Fe+H2SO4→FeSO4+H2
2Al+3H2SO4→Al2(SO4)3+3H2
⇒x+3y/2=0,105 (1)
P2:
2Fe+6H2SO4→3SO2+Fe2(SO4)3+6H2O2
2Al+6H2SO4→3SO2+Al2(SO4)3+6H2O
2Ag+2H2SO4→SO2+Ag2SO4+2H2O
⇒3x/2+3y/2+z/2=0,13 (2)
mà 56x+27y+108z=10,38:2 (3)
Từ (1),(2),(3) ⇒x=0,03; y=0,05; z=0,02 mol
Khi đó: mFe=2.56.0,03=3,36 g; mAl=2.27.0,05=2,7 g
mAg=2.108.0,02=4,32 g
Vì phần 1 tác dụng với H2SO4 loãng => sinh ra khí H2
=> n H2 = 0,105 ( mol )
Có: n SO2 = 0,13 ( mol )
Gọi n Fe, n AL, n Ag ở mỗi phần lần lượt là a, b, c
Vì m Fe + m Al + m Ag = 10,38
=> 56a + 27b + 108c = 10,38 : 2 = 5,19 ( 1 )
PTHH của phần 1
Fe + H2SO4 ====> FeSO4 + H2
2Al + 3H2SO4 =====> Al2(SO4)3 + 3H2
theo pthh: a+ 1,5b = 0,105 ( mol ) ( 2 )
PTHH của phần 2
2Fe + 6H2SO4 =====> Fe2(SO4)3 + 3SO2 + 6H2O
2AL + 6H2SO4 ===> Al2(SO4)3 + 3SO2 + 6H2O
2Ag + 2H2SO4 =====> Ag2SO4 + SO2 + 2H2O
theo PTHH: 1,5a + 1,5b + 0,5c = 0,13 ( 3 )
từ ( 1 ) , (2) và (3) suy ra
a = 0,03 ( mol ) => m Fe = 3,36 ( g )
b = 0,05 ( mol ) => m Al = 2,7 ( g )
c = 0,02 ( mol ) => m Ag = 4,32 ( g )

\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_{H_2SO_4}=0,15.2=0,3mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 < 0,3 ( mol )
0,2 0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
\(m_{FeSO_4}=0,2.152=30,4g\)
\(\left\{{}\begin{matrix}C_{M_{FeSO_4}}=\dfrac{0,2}{0,15}=1,33M\\C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,3-0,2}{0,15}=0,67M\end{matrix}\right.\)
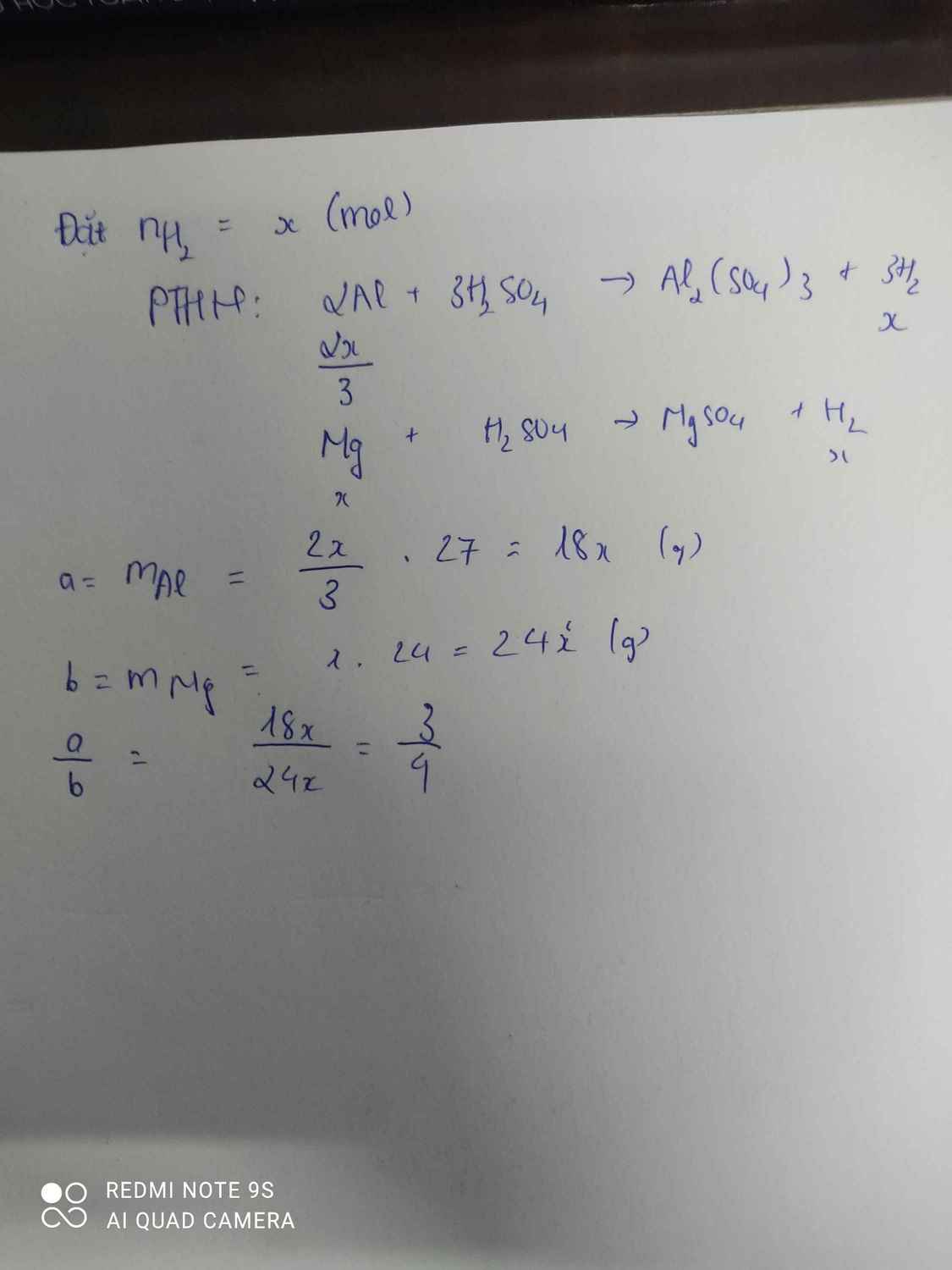
Giả sự đều sinh ra 1 mol H2
2Al+3H2SO4--->Al2(SO4)3+3H2
2/3_______________________1
=>a=2/3.27=18
Zn+H2SO4--->ZnSO4+H2
1___________________1
=>b=65
===> a/b=18/65