Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

5.
\(n_X=\dfrac{2,24}{22,4}=0,1mol\\ M_X=2,125.4=8,5g\cdot mol^{^{ }-1}\\ n_{H_2}=a;n_{C_2H_4}=b\\ a+b=0,1\\ 2a+28b=8,5.0,1=0,85\\ a=0,075;b=0,025\\ H_2+C_2H_4-^{^{ }Ni,t^{^{ }0}}->C_2H_6\\ V_{C_2H_6}=0,025.22,4=0,56L;V_{H_2dư}=22,4\left(0,075-0,025\right)=1,12L\)
6.
Thu được Y chỉ gồm hydrocarbon nên khí hydrogen phản ứng hết.
\(n_A=\dfrac{4,48}{22,4}=0,2mol\\ n_Y=\dfrac{3,36}{22,4}=0,15mol\\ \Delta n_{hh}=n_{H_2\left(pư\right)}=0,05\left(mol\right)\\ n_{C_2H_4}=0,15\left(mol\right)\\ a.\%V_{H_2}=\dfrac{0,05}{0,2}=25\%\\ \%V_{C_2H_4}=75\%\\ b.BTLK\pi:0,15=0,05+n_{Br_2}\\ n_{Br_2}=0,1mol\)

a. Phương trình phản ứng giữa axetilen và dung dịch Br2:
C2H2 + Br2 → C2H2Br2
b. Theo định luật Avogadro, số mol khí thể tích bằng nhau ở cùng điều kiện nhiệt độ và áp suất. Vì vậy, số mol của hỗn hợp Y bằng số mol của khí thoát ra sau phản ứng.
Theo đó, ta có thể tính số mol mỗi khí trong hỗn hợp:
Số mol khí thoát ra: n = V/ Vm = 2,24/ 22,4 = 0,1 molSố mol axetilen ban đầu: n(C2H2) = n = 0,1 molSố mol metan ban đầu: n(CH4) = (V(Y) - V(C2H2)) / Vm = (3,36 - 2,24) / 22,4 = 0,05 molc. Để tính % về khối lượng từng khí trong hỗn hợp, ta cần biết khối lượng riêng của từng khí. Ở đktc, khối lượng riêng của axetilen là 1,096 g/L và khối lượng riêng của metan là 0,717 g/L.
Khối lượng axetilen trong hỗn hợp: m(C2H2) = n(C2H2) x M(C2H2) = 0,1 x 26 = 2,6 gKhối lượng metan trong hỗn hợp: m(CH4) = n(CH4) x M(CH4) = 0,05 x 16 = 0,8 gTổng khối lượng của hỗn hợp Y: m(Y) = V(Y) x ρ(Y) = 3,36 x 1,25 = 4,2 gVậy, % về khối lượng của axetilen trong hỗn hợp là:
% m(C2H2) = (m(C2H2) / m(Y)) x 100% = (2,6 / 4,2) x 100% = 61,9%
% về khối lượng của metan trong hỗn hợp là:
% m(CH4) = (m(CH4) / m(Y)) x 100% = (0,8 / 4,2) x 100% = 19,0%

a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
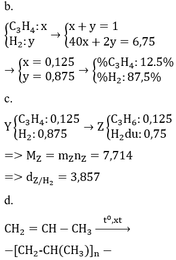


\(\overline{M}=24\cdot2=48\)
\(\dfrac{n_{SO_2}}{n_{O_2}}=\dfrac{64-48}{48-32}=1\)
\(n_{hh}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(\Rightarrow n_{SO_2}=n_{O_2}=0.15\left(mol\right)\)
\(2SO_2+O_2\underrightarrow{^{t^0,V_2O_5}}2SO_3\)
Bđ:0.15....0.15
Pư: x..........0.5x......x
KT: 0.15-x..0.15-0.5x..x
\(n_{hh}=0.15-x+0.15-0.5x+x=0.3-0.5x\left(mol\right)\)
\(m=\left(0.15-x\right)\cdot64+\left(0.15-0.5x\right)\cdot32+80x=\left(0.3-0.5x\right)\cdot2\cdot26\)
\(\Rightarrow x=\dfrac{3}{65}\)
\(H\%=\dfrac{\dfrac{3}{65}}{0.15}\cdot100\%=30.7\%\)

Tính nX= 0,8 mol; nZ= 0,3 mol; MY= 29 g/mol; MZ= 18,3332 g/mol
MX= \(\dfrac{\text{44.1 + 52.1+40.3+28.2+2.9}}{16}\) = 18,125 g/mol
Các hidrocacbon không no đều có chỉ số H= 4 nên đặt công thức chung là CxH4.
*Phản ứng của X với Ni nung nóng:
CxH4+ y H2 → CxH4+2y (1)
Theo bảo toàn khối lượng ta có: mY= mX= 0,8.18,125= 14,5 gam
→ nY= 14,5 : 29= 0,5 mol
Theo phản ứng (1) thấy số mol khí giảm xuống bằng số mol H2 phản ứng
Vậy nH2 phản ứng= 0,8- 0,5= 0,3 mol
*Phản ứng của Y với dung dịch Br2 dư:
Y gồm Z (C3H8, C2H6, C4H10) và các hidrocacbon không no: CnHm
CnHm+ a Br2 → CnHmBr2a (2)
Khối lượng bình brom tăng lên bằng khối lượng hidrocacbon không no trong Y
Bảo toàn khối lượng ta có: mZ+ mCnHm= mY
Nên mbình brom tăng= mCnHm= mY- mZ= 14,5- 0,3.4.4,5833= 9 gam
Xét cả quá trình thì toàn bộ liên kết kém bền đều bị đứt hết
Đặt công thức chung của H2 phản ứng và Br2 phản ứng là X2.
C4H4+ 3X2 → C4H4X6
C3H4+ 2X2 → C3H4X4
C2H4+ X2 → C2H4X2
Tổng số mol liên kết kém bền trong X là n
Ta có: nX2= 3.nC4H4+ 2.nC3H4 + nC2H4= 3.1+2.3+216.0,8=0,55(mol)
Nên nBr2 pứ= nX2- nH2 pứ= 0,55- 0,3= 0,25 mol

trong 1 mol hh ban đầu có nH2 =0,75 mol , nC2H4 =0,25 mol
nsau= 2,125.13/34=0,8125
=> nH2 pứ =ntrc -nsau =1- 0.8125=0,1875
=> H= 0,1875/0,75 .100= 25%

Ta có: \(n_Y=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow M_Y=\dfrac{1,32}{0,1}=13,2\left(g/mol\right)\)
→ Y gồm H2 dư và C2H6.
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2\left(dư\right)}+n_{C_2H_6}=0,1\\2n_{H_2\left(dư\right)}+30n_{C_2H_6}=1,32\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{H_2\left(dư\right)}=0,06\left(mol\right)\\n_{C_2H_6}=0,04\left(mol\right)\end{matrix}\right.\)
Gọi: \(\left\{{}\begin{matrix}n_{H_2}=x\left(mol\right)\\n_{C_2H_2}=n_{C_2H_4}=y\left(mol\right)\end{matrix}\right.\)
BTNT C: 2y = 0,04 ⇒ y = 0,02 (mol)
Có: nH2 (pư) = 2nC2H2 + nC2H4 = 0,06 (mol)
⇒ nH2 = 0,06 + 0,06 = 0,12 (mol)
\(\Rightarrow V=\left(0,12+0,02+0,02\right).22,4=3,584\left(l\right)\)