Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cl2 + 2NaI → 2NaCl + I2
nI2 = 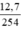 = 0,05 mol.
= 0,05 mol.
Theo pt: nCl2 = nI2 = 0,05 mol.
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
nHCl = 4. nCl2 = 4. 0,05 = 0,2 mol.
Khối lượng HCl cần dùng là: mHCl = 0,2 x 36,5 = 7,3g.

Đáp án B
Phương trình hóa học của phản ứng
Cl2 + 2NaI → 2NaCl + I2
0,05 ← 0,05 (mol)
nIot = 0,05 mol
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
0,2 ← 0,05 (mol)
Khối lượng HCl cần dùng là: mHCl = 0,2 x 36,5 = 7,3g

| 4HCl | + | MnO2 | → | Cl2 | + | 2H2O | + | MnCl2 |
0,2 <======= 0,05
| Cl2 | + | 2NaI | → | I2 | + | 2NaCl |
0,05 <========12,7/254
ta có:
mHCl= 0,2 *36,5=7,3g

3)Phương trình hóa học của phản ứng:
Cl2 + 2NaI → 2NaCl + I2
71g (2 x 127)g
X g 12,7g
X = 3,55g
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
(4 x 36,5g) 71g
Y g 3,55 g
Y = 7,3g
Khối lượng HCl cần dùng là 7,3g
1)
nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol. 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) = CM(MnCl2) = CM(NaClO) = 0,8 /0,5 = 1,6 mol/l
CM(NaOH)dư = (2. 1,6)/0,5 = 0,8 mol/l

Phương trình hóa học của phản ứng:
Cl2 + 2NaI → 2NaCl + I2
71g (2 x 127)g
X g 12,7g
X = 3,55g
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
(4 x 36,5g) 71g
Y g 3,55 g
Y = 7,3g
Khối lượng HCl cần dùng là 7,3g

PT: \(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
Ta có: \(n_{HCl}=0,025.8=0,2\left(mol\right)\)
Theo PT: \(n_{Cl_2}=\dfrac{1}{4}n_{HCl}=0,05\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=0,05.22,4=1,12\left(l\right)\)
Bạn tham khảo nhé!
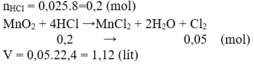
MnO2+4HCl->MnCl2+2H2O+Cl2
...........0,4----------------------------0,1
Cl2+2NaI->2NaCl+I2
0,1----------------------0,1
nI=12,7\127=0,1 mol
=>mHCl=0,4.36,5=14,6g
\(MnO_2+4HCl\underrightarrow{^{to}}MnCl_2+Cl_2+2H_2O\left(1\right)\)
\(Cl_2+2NaI\rightarrow NaCl+I_2\left(2\right)\)
\(n_{I2}=\frac{12,7}{254}=0,05\left(mol\right)\)
\(\Rightarrow n_{Cl2}=n_{I2}=0,05\left(mol\right)\)
Dựa vào PT (1), ta thấy:
\(n_{HCl}=4n_{Cl2}=0,05.4=0,2\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,2.36,5=7,3\left(g\right)\)