cho 8 g sulfur trioxide tác dụng hết với dung dịch naoh loãng dư thu được muối sodium sulfate (na2so4) và nước khối lượng naoh tham gia phản ứng và khối lượng muối thu được lần lượt là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) $n_{H_2SO_4} = \dfrac{490.10\%}{98} = 0,5(mol)$
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
Theo PTHH :
$n_{NaOH} = 2n_{H_2SO_4} = 1(mol)$
$\Rightarrow m_{dd\ NaOH} = \dfrac{1.40}{20\%} = 200(gam)$
\(n_{H_2SO_4}=\dfrac{490.10\%}{98}=0,5\left(mol\right)\\ 2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ n_{NaOH}=0,5.2=1\left(mol\right)\\ m_{ddNaOH}=\dfrac{1.40.100}{20}=200\left(g\right)\)

a, \(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
b, \(n_{H_2SO_4}=0,2.1,5=0,3\left(mol\right)\)
Theo PT: nNa2SO4 = nH2SO4 = 0,3 (mol) ⇒ mNa2SO4 = 0,3.142 = 42,6 (g)
nNaOH = 2nH2SO4 = 0,6 (mol) ⇒ mNaOH = 0,6.40 = 24 (g)
c, \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(\Rightarrow\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,6}{0,4}=1,5\) → Pư tạo NaHCO3 và Na2CO3.
PT: \(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(NaOH+CO_2\rightarrow NaHCO_3\)

Chọn đáp án A
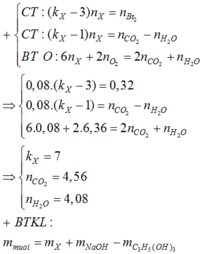
= 4 , 56 . 12 + 4 , 08 . 2 + 0 , 08 . 6 . 16 + 0 , 08 . 3 . 40 - 0 , 08 . 92
= 72 , 8 g a m

Ta có nBr2 : nX = 0,32 : 0,08 = 4 nên các gốc hiđrocacbon của chất béo có tổng cộng 4π
Mà mỗi gốc COO có 1π nên độ bất bão hòa của toàn phân tử X là k = 4 + 3 = 7
- Phản ứng đốt 0,08 mol X:
Giả sử nCO2 = a và nH2O = b (mol)
+) Bảo toàn O → 6nX + 2nO2 = 2nCO2 + nH2O
→ 2a + b = 6.0,08 + 2.6,36 (1)
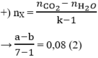
Giải (1) (2) được a = 4,56 và b = 4,08
BTKL → mX = mCO2 + mH2O - mO2 = 4,56.44 + 4,08.18 - 6,36.32 = 70,56 gam
Ta có X + 3NaOH → Muối + C3H5(OH)3
0,08 → 0,24 → 0,08 (mol)
BTKL → mmuối = mX + mNaOH - mC3H5(OH)3
= 70,56 + 0,24.40 - 0,08.92 = 72,8 gam
Đáp án cần chọn là: A

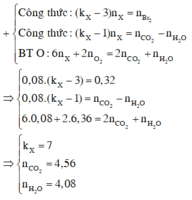

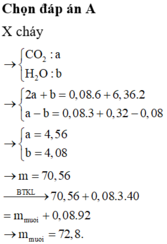
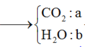
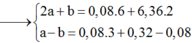
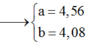
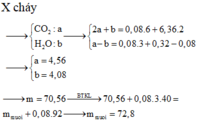
\(SO_3+2NaOH\rightarrow Na_2SO_4+H_2O\\ n_{SO_3}=\dfrac{8}{40}=0,2\left(mol\right)\Rightarrow n_{Na_2SO_4}=n_{SO_3}=0,2\left(mol\right);n_{NaOH}=2.0,2=0,4\left(mol\right)\\ m_{NaOH}=0,4.40=16\left(g\right);m_{Na_2SO_4}=142.0,2=28,4\left(g\right)\)