Hòa tan m gam Fe vào 300 ml dung dịch H2SO4 0,5M thu được dung dịch X và V1 lít H2 ở đktc. Cho dung dịch X tác dụng vừa đủ với V2 ml dung dịch Ba(OH)2 1M thu được 41,7 gam kết tủa. Tính m, V1, V2.
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

16 tháng 12 2017
Định hướng tư duy giải
Ta có:
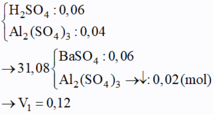
Thêm tiếp Ba(OH)2 kết tủa bị tan 1 phần
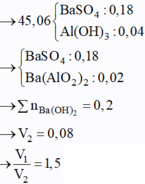

22 tháng 8 2018
Chọn đáp án B
Xét thí nghiệm 1: 3Ba(OH)2 + Al2(SO4)3 → 3BaSO4 + 2Al(OH)3.
Giả sử
![]()
Phản ứng vừa đủ ⇒ n B a ( O H ) 2 = 3 V 1
![]()
![]()
⇒ 0 , 9 m = 769 , 5 V 1 g a m
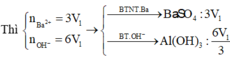
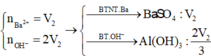
s TH1: Ba(OH)2 thiếu. n B a ( O H ) 2 = V 2 mol
![]()
![]()
![]()
s TH2: Ba(OH)2 dư, hòa tan 1 phần Al(OH)3. Khi đó:
3Ba(OH)2 + Al2(SO4)3 → 3BaSO4 + 2Al(OH)3 (1)
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O (2)
Từ (1)
![]()
![]()
![]()
![]()
![]()
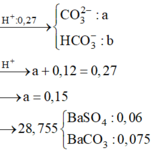
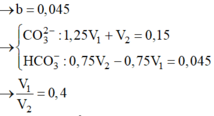

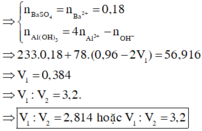
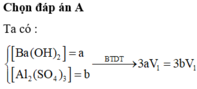
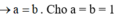


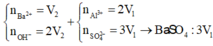
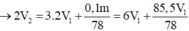
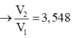



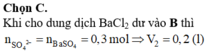

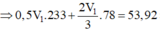
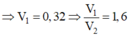
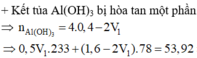

PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(FeSO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+Fe\left(OH\right)_2\downarrow\)
Ta có: \(n_{H_2SO_4}=0,3\cdot0,5=0,15\left(mol\right)=n_{Fe}=n_{H_2}=n_{Ba\left(OH\right)_2}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,15\cdot56=8,4\left(g\right)\\V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\\V_{Ba\left(OH\right)_2}=\dfrac{0,15}{1}=0,15\left(l\right)=150\left(ml\right)\end{matrix}\right.\)
*Bạn xem lại đề vì nếu FeSO4 p/ứ hết thì sẽ có nhiều hơn 41,7 gam kết tủa
H2SO4 dư bạn