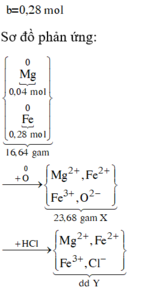
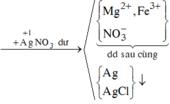
Đốt cháy 16,64 gam hỗn hợp gồm Mg và Fe trong khí O2, thu được 23,68 gam hỗn hợp X chỉ gồm các oxit.Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 24 gam chất rắn. Mặt khác cho Y tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là
A. 126,28
B. 128,44
C. 130,6
D. 43,20


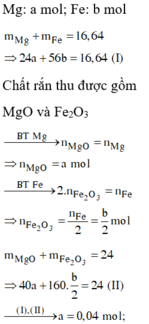




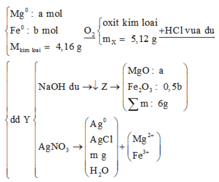
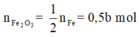
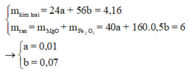
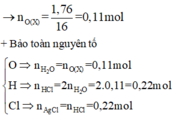
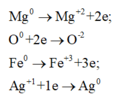
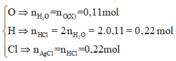
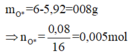
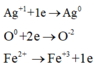
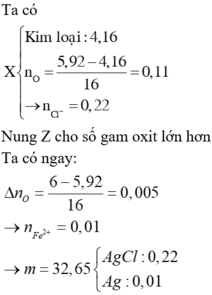

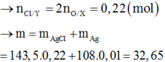
Đáp án : C
Đặt nMg = x ; nFe = y
=> 24x + 56y = 16,64g
Và 40x + 80y = 24
=> x = 0,04 ; y = 0,28
nCl = 2nO = 2. 23 , 68 - 16 , 64 16 = nAgCl
Bảo toàn e : 0,04.2 + 0,28.3 = 2.0,44 + nAg+
=> nAg+ = 0,84 mol
=> m = 0,04 .108 + 0,88.143,5 = 130,6