Đốt cháy hoàn toàn 13 gam một kim loại hóa trị II trong oxi dư đến khối lượng không đổi thu được 16,2 gam chất rắn X. Kim loại đó là:
A. Zn
B. Fe
C. Cu
D. Ca
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Câu 1 :
Gọi X lak tên kim loại đó
Theo đề ra ta có : \(2X+O_2\left(t^o\right)->2XO\)
Ta có : \(n_{XO}=\dfrac{16,2}{M_X+16}\); \(n_X=\dfrac{13}{M_X}\)
Từ PT -> \(n_X=n_{XO}\)
=> \(\dfrac{16,2}{M_X+16}=\dfrac{13}{M_X}\)
Giải phương trình trên ta đc \(M_X=65\left(g/mol\right)\)
-> Kim loại đó lak Zn
Câu 2 :
PTHH : \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(n_{O_2}=\dfrac{V\left(đktc\right)}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Từ PT -> \(n_P=\dfrac{4}{5}n_{O_2}=0,08\left(mol\right)\)
-> \(m_{P\left(PƯđủ\right)}=n.M=0,08.31=2,48\left(g\right)\)

\(GọinlàhóatrịcủaX\\ PTHH:2X+nO_2-^{t^o}\rightarrow X_2O_n\\ Tacó:n_X=2n_{X_2O_n}\\ \Rightarrow\dfrac{12,15}{X}=2.\dfrac{22,95}{2X+16n}\\ Chạynghiệmn:\\ n=1\Rightarrow X=9\\ n=2\Rightarrow18\\ n=3\Rightarrow X=27\left(chọn-Al\right)\\ \Rightarrow ChọnD\)

Đáp án B.
Gọi kim loại là R.
Bảo toàn khối lượng:
mO = 16,2 - 13 = 3,2
=> nO2= 0,1 (mol)
2R + O2→ 2RO
0,2 0,1
MR = 65(Zn)

Đáp án A
Các phản ứng có thể xảy ra:
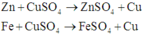
Trong 3 kim loại Zn, Fe và Cu thì Fe có khối lượng mol nhỏ nhất
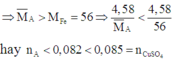
Do đó B chứa Cu2+ dư
Khi đó C chứa Cu trong A và Cu sinh ra sau phản ứng. Nên D chứa CuO.
B chứa Zn2+, Fe2+ và Cu2+ dư. Khi cho B tác dụng với dung dịch NaOH dư thì kết tủa thu được chứa Fe(OH)2 và Cu(OH)2 .
Do đó E chứa Fe2O3 và CuO.
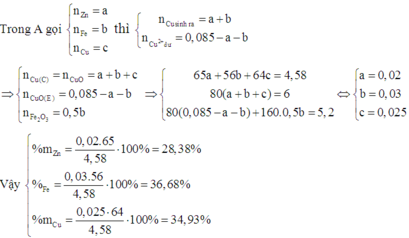

Chọn đáp án D
M + C l 2 → t 0 M C l 2
n M = n M C l 2 ⇒ 7 , 2 M = 28 , 5 M + 71
=> M = 24 (Mg)

Đáp án D.
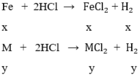
gọi x, y lần lượt là số mol của Fe và M trong hỗn hợp
số mol H2 là 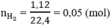
theo bài ra ta có hệ phương trình
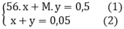
từ (2) → x= 0,05 – y
thay vào (1) ta được 56(0,05 – y) + My = 0,5
⇔ 2,8 – 56y + My = 0,5
2,3 = 56y – My
→ y = 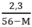
Ta có 0 < y < 0,05
y > 0 ↔ 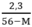 > 0 → 56 – M > 0 ⇒ M < 56
> 0 → 56 – M > 0 ⇒ M < 56
y < 0,05 ↔ 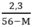 < 0,05 → 2,3 < 0,05(56 – M) → M < 10
< 0,05 → 2,3 < 0,05(56 – M) → M < 10
Trong các kim loại hóa trị II chỉ có Be thỏa mãn do đó M là Be

Bảo toàn khối lượng: mO2 = mRO - mR = 32,4 - 26 = 6,4 (g)
\(n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\)
PTHH: 2R + O2 --to--> 2RO
\(M_R=\dfrac{26}{0,2}=65\left(\dfrac{g}{mol}\right)\)
=> R là Zn