Sục V lít CO2 vào 300ml dung dịch KOH 1M, sau phản ứng kết thúc thu được dung dịch có chứa 26,9 g muối. Tính V (đktc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


đâu phải bài nào đưa lên cx xong luôn đc. Với lại bài bn ms đưa lên đc có 2 phút thì bn lại lm xong rồi còn gì

\(n_{KOH}=0.3\cdot1=0.3\left(mol\right)\)
Giả sử phản ứng CO2 với KOH vừa đủ để tạo thành K2CO3 :
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\left(1\right)\)
\(n_{K_2CO_3}=\dfrac{0.3}{2}=0.15\left(mol\right)\)
\(m_{K_2CO_3}=0.15\cdot138=20.7\left(g\right)< 26.9\left(g\right)\)
=> Tạo sản phẩm có 2 muối
\(n_{CO_2\left(1\right)}=x\left(mol\right)\)
\(n_{CO_2\left(2\right)}=y\left(mol\right)\)
\(KOH+CO_2\rightarrow KHCO_3\left(2\right)\)
\(\left\{{}\begin{matrix}2x+y=0.3\\138x+100y=26.9\end{matrix}\right.\)
\(\left\{{}\begin{matrix}x=0.05\\y=0.2\end{matrix}\right.\)
\(V=0.25\cdot22.4=5.6\left(l\right)\)
\(n_{KOH}\)\(=0,3mol\)
Giả sử phản ứng tạo ra K2CO3 và KHCO3
Đặt \(n_{K_2CO_3}=a\) mol ,\(n_{KHCO_3}=b\) mol
PTHH 2KOH+CO2→K2CO3+H2O (1)
KOH+CO2→KHCO3 (2)
Theo pt (1)(2): \(n_{KOH}=2n_{K_2CO_3}+n_{KHCO_3}=2a+b=0,3\)(*)
\(m^{ }_{Muối}\) = \(m_{K_2CO_3}+m_{KHCO_3}=26,9\left(g\right)\)
=> 138a+100b=26,9(**)
Từ (*)(**) giải hệ phương tình ta có\(\left\{{}\begin{matrix}a=0,05\\b=0,2\end{matrix}\right.\)
Theo pt (1)(2):\(\Sigma_{n_{CO_2}}=a+b=0,05+0,2=0,25\) mol
=>\(V_{CO_2}=5,6\left(l\right)\)
Nếu bài cho dd chứa muối thì bạn làm kiểu này không cần xác định ra muối nào nha,nếu nó ra 1 muối thì sẽ có 1 ẩn bằng 0

Đáp án B
Ta có :
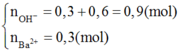
Vì cho BaCl2 vào X có kết tủa nên X có dư
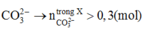
Tất nhiên ta có thể thử đáp án. Tuy nhiên, tôi sẽ biện luận với 2 trường hợp có thể xảy ra với X vẫn thỏa mãn đầu bài là :
+ Nếu X chỉ chứa
![]()
![]()
+ Nếu X chứa
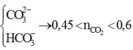
![]()



| CHÚ Ý |
| Với bài toán sục khí CO2 vào dung dịch kiềm. Nếu quá trình tạo muối có sinh ra dưới dạng muối tan và kết tủa. Ví dụ như BaCO3 và Na2CO3 thì khi tiếp tục sục khí CO2 vào thì Na2CO3 sẽ phản ứng với CO2 trước. Khi hết Na2CO3 rồi thì kết tủa BaCCO3 mới bị hòa tan. |

n OH = 0,4 + 0,2.2 = 0,8(mol)
n CO3 2- = x(mol) ; n HCO3 - = y(mol)
Ta có :
x + y = 0,5
2x + y = 0,8
=> x = 0,3 ;y = 0,2
Ba2+ + CO32- → BaCO3
0,2.......0,2............................(mol)
Vậy dung dịch gồm :
K+ : 0,4(mol)
CO3 2- : 0,3 - 0,2 = 0,1(mol)
HCO3 - : 0,2(mol)
n HCl = a(mol) => n H2SO4 = 0,5a(mol)
=> n H+ = 2a(mol)
Gọi n CO3 2- pứ = 0,1b => n HCO3- pư = 0,2b(mol)
Ta có :
n H+ = 0,1b.2 + 0,2b
=> 0,4b = 2a
Sau phản ứng :
Bảo toàn nguyên tố với C :
n BaCO3 = 0,2 + 0,1 - 0,1b - 0,2b = 0,3 - 0,3b
Ta có :
0,5a.233 + (0,3 - 0,3b).197 = 41,2
=> a = 0,1 ; b = 0,05
=> n CO2 = 3b = 0,15
=> V = 3,36 lít
Mk muốn đc joir tại sao nH+=0.1b×2 + 0.2b
Bạn bảo toàn gì hay sao, giải thích giúp mk với




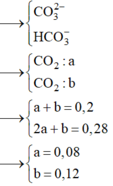
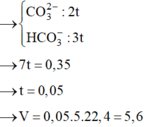
nKOH=0.3⋅1=0.3(mol)
Giả sử phản ứng CO2 với KOH vừa đủ để tạo thành K2CO3 :
2KOH+CO2→K2CO3+H2O(1)
nK2CO3=\(\dfrac{0.3}{2}\)=0.15(mol)
mK2CO3=0.15⋅138=20.7(g)<26.9(g)
⇒ Tạo sản phẩm có 2 muối
nCO2(1)=x(mol)
nCO2(2)=y(mol)
KOH+CO2→KHCO3(2)
\(\left\{{}\begin{matrix}\text{2 x + y = 0.3 }\\\text{138 x + 100 y = 26.9}\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\text{x = 0.05}\\\text{y = 0.2}\end{matrix}\right.\)
V=0.25⋅22.4=5.6(l)