đun nóng 8,1g Al và 9,6g S trong môi trường kín không có không khí thu được hỗn hợp X. cho X phản ứng hoàn toàn với dd HCl thu được hỗn hượp khí A
a) tính tỉ khối của hỗn hợp khí A so với không khí, so với H2
b) dẫn khí A qua dd Pb(NO3)2 0,5M. tính khối lượng kết tủa thu được và thể tích dd Pb(NO3)2 vừa đủ dể phản ứng với lượng khí dẫn vào
c) dẫn khí Aqua 400ml dd KOH2M. tính nồng độ mol của dd thu được sau phản ứng



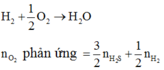
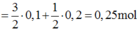



PTHH: 2Al + 3 S -----to----> Al2S3
\(n_{Al}=\frac{8,1}{27}=0,3\left(mol\right);n_S=\frac{9,6}{32}=0,3\left(mol\right)\)
Lập tỉ lệ Al và S : \(\frac{0,3}{2}>\frac{0,3}{3}\) => Sau phản ứng Al dư, S phản ứng hết
Theo PT: \(n_{Al\left(p.ứ\right)}=\frac{2}{3}n_S=0,2\left(mol\right)\)
n Al2S3 = \(\frac{1}{3}n_S=0,1\left(mol\right)\)
nAl dư = nAl bđ - n Al p/ứ = 0,3 - 0,2 =0,1 (mol)
=>X gồm Al dư, Al2S3
2Al +6 HCl ---------> 2AlCl3 + 3H2 (*)
Al2S3 + 6HCl -------> 2AlCl3 +3 H2S (**)
Hỗn hợp khí A: H2 , H2S
Theo PT (*) \(n_{H_2}=\frac{3}{2}n_{Al}=0,15\left(mol\right)\)
\(n_{H_2S}=3n_{Al_2S_3}=0,3\left(mol\right)\)
\(M_{hhA}=\frac{0,15.2+0,3.34}{0,15+0,3}=\frac{70}{3}\)
dA/kk\(=\frac{\frac{70}{3}}{29}=\frac{70}{87}\approx0,8\)
dA/H2\(=\frac{\frac{70}{3}}{2}=\frac{35}{3}\approx11,67\)
b) Khí dẫn vào là H2, H2S nhưng chỉ có H2S phản ứng
Pb(NO3)2 + H2S -------> PbS + 2HNO3
Theo PT : n PbS = nH2S =0,3 (mol)
\(\Rightarrow m_{PbS}=0,3.239=71,7\left(g\right)\)
n Pb(NO3)2 = nH2S =0,3 (mol)
\(\Rightarrow V_{Pb\left(NO_3\right)_2}=\frac{0,3}{0,5}=0,8\left(l\right)\)
b) Khí dẫn vào là H2, H2S nhưng chỉ có H2S phản ứng
2KOH + H2S ------> K2S +2 H2O
\(n_{KOH}=2.0,4=0,8\left(mol\right)\)
Lập tỉ lệ KOH và H2S: \(\frac{0,8}{2}>\frac{0,3}{1}\)=> KOH dư, H2S phản ứng hết
Dung dịch sau phản ứng gồm K2S và KOH dư
Theo PT: nKOH p/ứ = 2n H2S = 0,6(mol)
=> n KOH dư = 0,8 - 0,6 =0,2 (mol)
Theo PT: nK2S = n H2S = 0,3(mol)
\(\Rightarrow C_{M\left(KOH_{dư}\right)}=\frac{0,2}{0,4}=0,5M\)
\(C_{M\left(K_2S\right)}=\frac{0,3}{0,4}=0,75M\)
nAl = 8,1/27 = 0,3 mol ; nS = 9,6/32 = 0,3 mol
PTHH :
2Al + 3S --to--> Al2S3
nAl phản ứng = 2/3 . nS = 0,3.2/3 = 0,2 mol
=> nAl dư = 0,3 -0,2 = 0,1 mol
có nAl2S3 = 1/3 . nS = 0,1 mol
PTHH :
2Al + 6HCl → 2AlCl3 + 3H2
0,1 _________________0,15 (mol)
Al2S3 + 6HCl → 2AlCl3 + 3H2S
0,1_______________________0,3 (mol)
Từ PT , có nH2 = 0,15 mol ; nH2S = 0,3 mol
\(M_A=\frac{0,15.2+0,3.34}{0,3+0,15}=23,33\left(\frac{g}{mol}\right)\)
\(\Rightarrow d_{A/H2}=\frac{23,33}{2}=11,67\)
b,
nH2S = 0,3 mol
PTHH : Pb(NO3)2 + H2S → PbS + 2HNO3
_______ 0,3_________0,3______0,3 _________
Theo PT , nPb(NO3)2 = nPbS = 0,3 mol
=> mPbS = 0,3.239 = 71,7 gam
=> V Pb(NO3)2 = 0,3/0,5 = 0,6M
c,
nKOH = 0,4.2 =0,8 mol
có nKOH/nH2S = 0,8/0,3 = 2,67 > 2 nên KOH dư , muối có K2S
PTHH :
2KOH + H2S → K2S + 2H2O
0,6 ___0,3______0,3_____________
nKOH phản ứng = 0,6 mol ; nK2S = 0,3 mol
=> nKOH dư = 0,8-0,6 =0,2 mol
=> CM KOH dư = 0,2/0,4 =0,5M ; CM K2S = 0,3/0,4 = 0,75M