Đề thi HSG Hóa Học 9 Cấp Huyện
Bài 1: Nung 500 g đá vôi chứa 80% CaCO3 (phần còn lại là các oxit nhôm, sắt (III), silic), sau một thời gian thu được chất rắn X và V lít khí Y.
a, Tính khối lượng chất rắn X, biết hiệu suất phân hủy CaCO3 là 75%
b, Tính % khối lượng của CaO trong chất rắn X
c, Cho khí Y sục rất từ từ vào 800g dung dịch NaOH 2% thì thu được muối gì? Nồng độ bao nhiêu %?
Bài 2: Hỗn hợp A gồm BaO, FeO, Al2O3. Hòa tan A trong lượng nước dư được dung dịch D và phần không tan B. Sục khí CO2 dư vào D, phản ứng tạo kết tủa. Cho khí CO dư qua B nung nóng được chất rắn E. Cho E tác dụng với dung dịch NaOH dư, thấy tan một phần và còn lại là chất rắn G. Hòa tan hết G trong lượng dư dung dịch H2SO4 loãng rồi cho dung dịch thu được tác dụng với dung dịch KMnO4. Giải thích thí nghiệm trên bằng các phương trình phản ứng.
Bài 3: Cho một lá sắt có khối lượng 5g vào 50ml dung dịch CuSI4 15% có khối lượng là 1,12g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô, cân nặng 5,16g. Tính nồng độ % các chất còn lại trong dung dịch sau phản ứng
Bài 4: A là chất rắn khan. Cho m gam A vào dung dịch HCl 10%, khuấy đều được dung dịch B, ở đây không thấy tạo kết tủa hoặc bay hơi. Trong dung dịch B, nồng độ HCl là 6,1%. Cho NaOH vào dung dịch B để trung hòa hoàn toàn axit được dung dịch C. Cô cạn làm bay hơi hết nước trong dung dịch C người ta thu được duy nhất muối NaCl khan có khối lượng 16,03 g. A là chất nào? Tìm m
Bài 5: Nung m gam hỗn hợp X gồm 2 muối cacbonat trung hòa của 2 kim loại A, B đều có hóa trị II. Sau một thời gian thu được 3,36 lít khí CO2 (đktc), và còn lại hỗn hợp rắn Y
Cho Y tác dụng hết với dung dịch HCl dư, khí thoát ra hấp thụ hoàn toàn bởi dung dịch Ca(OH)2 dư thu được 15g kết tủa. Phần dung dịch đem cô cạn thu được 32,5g hỗn hợp muối khan. Viết PTPU xảy ra và tính m.
Bài 6: Dung dịch A0 chứa hồn hợp AgNO3 và Cu(NO3)2. Cho bột sắt vào A0, sau khi phản ứng xảy ra xong lọc tách được dung dịch A1, và chất rắn B1. Cho tiếp 1 lượng bột Mg vào dung dịch A1, kết thúc phản ứng lọc tách được dung dịch A2 và chất rắn B2 gồm 2 kim loại. Cho B2 vào dung dịch HCl không thấy hiện tượng gì nhưng khi hòa tan B2 bằng dung dịch H2SO4 đặc nóng thấy có khí SO2 thoát ra.
a, Viết PTHH xảy ra
b, Cho biết thành phần B1, B2 và các dung dịch A1, A2 là những chất gì?
Mọi người giúp em với ạ !!! Em xin cảm ơn trước ạ !!!


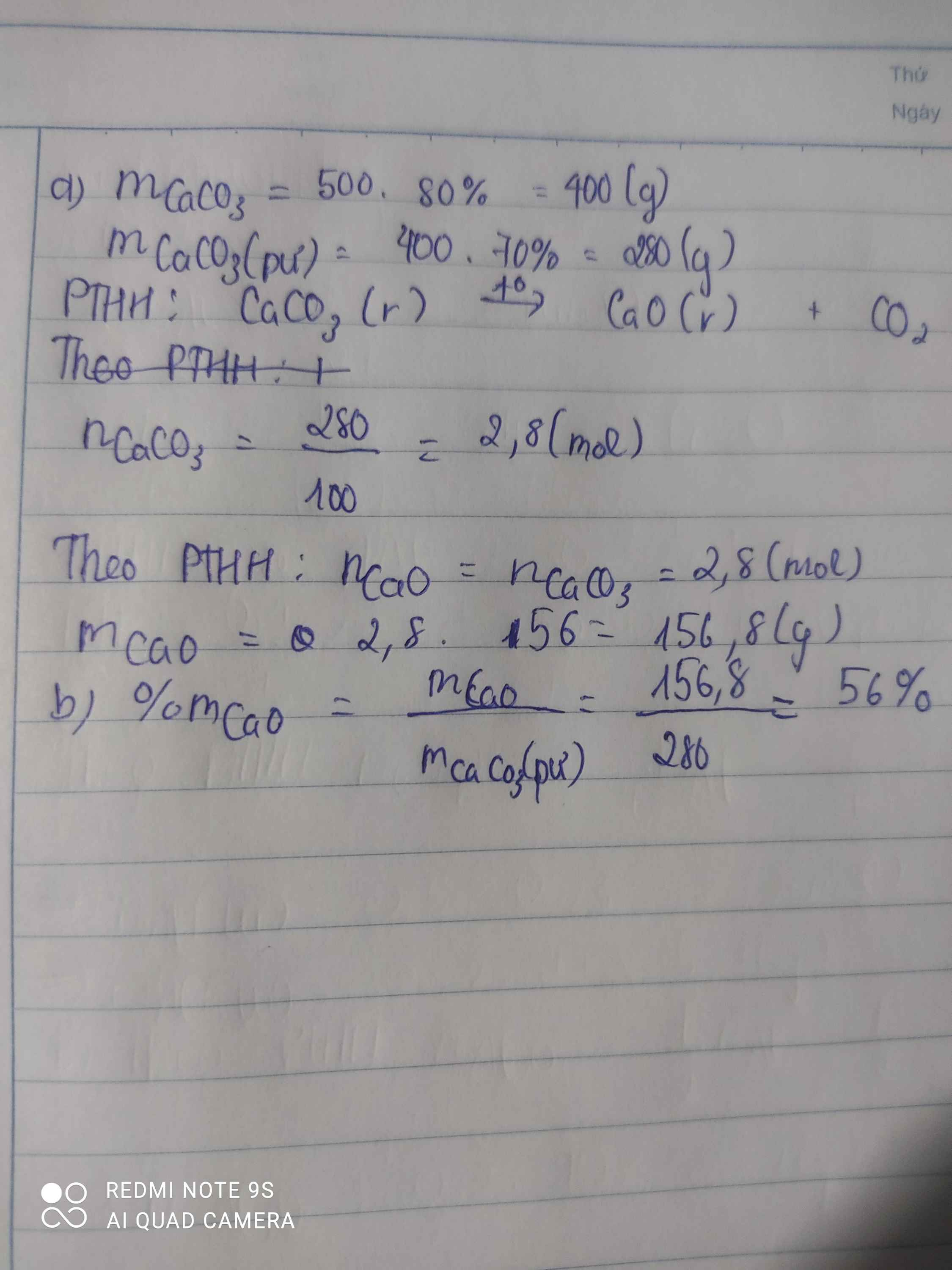
Bài 2: Hỗn hợp A gồm BaO, FeO, Al2O3. Hòa tan A trong lượng nước dư được dung dịch D và phần không tan B. Sục khí CO2 dư vào D, phản ứng tạo kết tủa. Cho khí CO dư qua B nung nóng được chất rắn E. Cho E tác dụng với dung dịch NaOH dư, thấy tan một phần và còn lại là chất rắn G. Hòa tan hết G trong lượng dư dung dịch H2SO4 loãng rồi cho dung dịch thu được tác dụng với dung dịch KMnO4. Giải thích thí nghiệm trên bằng các phương trình phản ứng.
________________________________________________________________________
A: BaO + FeO + Al2O3
B: FeO + Al2O3 dư
D: dd Ba(AlO2)2
E: Fe + Al2O3 dư
G: Fe
\(PTHH:BaO+H_2O\rightarrow Ba\left(OH\right)_2\)
\(Ba\left(OH\right)_2+Al_2O_3\rightarrow Ba\left(AlO_2\right)_2+H_2O\)
\(Ba\left(AlO_2\right)_2+4H_2O+2CO_2\rightarrow Ba\left(HCO_3\right)_2+2Al\left(OH\right)_3\)
\(FeO+CO\underrightarrow{t^o}Fe+CO_2\)
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(10FeSO_4+8H_2SO_4+2KMnO_4\rightarrow5Fe_2\left(SO_4\right)_3+8H_2O+2MnSO_4+K_2SO_4\)
Bài 3: Cho một lá sắt có khối lượng 5g vào 50ml dung dịch CuSO4 15% có khối lượng là 1,12g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô, cân nặng 5,16g. Tính nồng độ % các chất còn lại trong dung dịch sau phản ứng
_______________________________________________________________________
Gọi số mol Fe là x (mol)
\(PTHH:Fe+CuSO_4\rightarrow FeSO_4+Cu\)
(mol)_____x_____x_________x_____x__
(mol)
Theo đề bài ta có:
\(\Delta m=64x-56x=5,16-5\\ \Leftrightarrow8x=0,16\\ \Leftrightarrow x=0,02\left(mol\right)\)
\(m_{ddCuSO_4}=50.1,12=56\left(g\right)\\ n_{CuSO_4}=\frac{56.15}{100.160}=0,0525\left(mol\right)\)
Lập tỉ lệ: \(\frac{0,02}{1}< \frac{0,0525}{1}\rightarrow CuSO_4\) dư
\(m_{ddspu}=0,02.56+56-64.0,02=55,84\left(g\right)\)
\(C\%_{ddNaCl}=\frac{0,02.152}{55,84}.100\%=5,44\left(\%\right)\)
\(C\%_{ddCuSO_4\cdot du}=\frac{160.\left(0,0525-0,02\right)}{55,84}.100\%=9,31\left(\%\right)\)