cho 8 g lưu huỳnh trioxit tác dụng với nước ,thu được 250ml dung dịch axit sunfuric
a) viết phương trình hóa học
b)xác định nồng độ mol của dung dịch axit
c)nếu trung hòa hết lượng axit thu được ở trên bằng dung dịch KOH 5,6% có khối lượng riêng là 1,045 g/ml thì cần bao nhiêu ml dung dịch KOH ?

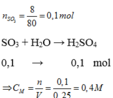
Ta có: \(n_{SO_3}=\dfrac{8}{80}=0,1\left(mol\right)\)
a. PTHH: SO3 + H2O ---> H2SO4 (1)
b. Theo PT(1): \(n_{H_2SO_4}=n_{SO_3}=0,1\left(mol\right)\)
Đổi 250ml = 0,25 lít
=> \(C_{M_{H_2SO_4}}=\dfrac{0,1}{0,25}=0,4\left(M\right)\)
c. PTHH: H2SO4 + 2KOH ---> K2SO4 + 2H2O
Theo PT(2): \(n_{KOH}=2.n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
=> \(m_{KOH}=0,2.56=11,2\left(g\right)\)
Ta có: \(C_{\%_{KOH}}=\dfrac{11,2}{m_{dd_{KOH}}}.100\%=5,6\%\)
=> \(m_{dd_{KOH}}=200\left(g\right)\)
Ta có: \(d_{KOH}=\dfrac{200}{V_{dd_{KOH}}}=1,045\)(g/ml)
=> \(V_{dd_{KOH}}=191,4\left(ml\right)\)