Trong bình kín chứa 0,5 mol CO và m gam Fe3O4, Đun nóng bình đến khi phản ứng hoàn toàn thì khí trong bình có tỉ khối so với khí CO ban đầu là 1,457. giá trị của m là:
A.16,8 gam
B. 9,4 gam
C. 22, 4 gam
D. 23,2 gam.
Em muốn hỏi là tại sao Fe3O4 phản ứng hết, nhưng sao ko gọi số mol của Fe3O4 là x rồi kéo qua mol của CO rồi tính tiếp mà lại gọi mol của CO là x rồi kéo qua những chất khác vậy ạ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D
Theo bài ra CO dư; F e 3 O 4 hết
Sau phản ứng có CO (đặt x mol) và C O 2 (đặt y mol)
Ta có n C O b đ = n C O d ư + n C O 2 → 0,5 = x + y (1)
m h h k h í = 0,5.1,457.28 = 20,4 gam → 28x + 44y = 20,4 (2)
Từ (1) và (2) có x = 0,1 và y = 0,4
PTHH:
4CO + F e 3 O 4 → 4 C O 2 + 3Fe
0,1 ← 0,4 mol
m = 0,1.232 = 23,2 gam.

Đáp án D
Do số mol FeO bằng số mol Fe2O3 nên ta có thể quy đổi hỗn hợp X thành Fe3O4
CO + Fe3O4 → CO2+ Chất rắn
Bản chất phản ứng:
CO + Ooxit→ CO2
x x x mol
Khí trong bình có chứa x mol CO2 và 0,5-x mol CO dư
→ M ¯ = m h h n h h = 44 x + 28 ( 0 , 5 - x ) x + 0 , 5 - x = 1 , 457 . 28
→x= 0,4 mol
4CO + Fe3O4 → t 0 3Fe + 4CO2
Theo PT: n F e 3 O 4 phản ứng = 1/4. nCO = 0,1 mol
→ m = m F e 3 O 4 = 0,1.232= 23,2 gam

Đáp án : B
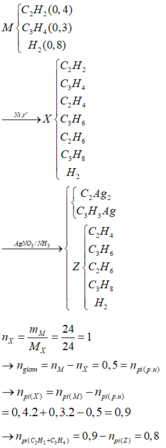
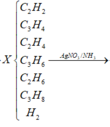
Theo BTKL: mX = 0,04 x 26 + 0,03 x 40 + 0,8 x 2 = 24 gam → nX = 24 : 24 = 1 mol.
Ta có nH2phản ứng = nhh ban đầu - nX = (0,4 + 0,3 + 0,8) - 1 = 0,5 mol.
nπ trước phản ứng = 2 x nCH≡CH + 2 x nCH≡C-CH3 = 2 x 0,4 + 2 x 0,3 = 1,4 mol.
→ nπ dư sau phản ứng = nπ trước phản ứng - nH2 = 1,4 - 0,5 = 0,9.
Mà nπ dư sau phản ứng = 2 x n↓ + nBr2 → n↓ = (0,9 - 0,1) : 2 = 0,4 mol.
Giả sử số mol của AgC≡CAg và AgC≡C-CH3 lần lượt là x, y mol
Ta có hpt: ![]()
→ m = 0,15 x 240 + 0,25 x 147 = 72,75 gam → Chọn C

\(n_{CO\ dư} = a(mol) ; n_{CO_2} = b(mol)\\ \Rightarrow a + b = \dfrac{4,48}{22,4} = 0,2(1)\\ m_{khí} = 28a + 44b = 20,4.2.0,2 = 8,16(gam)(2)\\ (1)(2) \Rightarrow a = 0,04 ; b = 0,16\\ Fe_3O_4 + 4CO \xrightarrow{t^o} 3Fe + 4CO_2\\ n_{Fe_3O_4} = \dfrac{1}{4}n_{CO_2} = 0,04(mol)\\ m_{Fe_3O_4} = 0,04.232 = 9,28(gam)\)
Ta có: \(\Sigma n_{CO}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(Fe_3O_4+4CO\underrightarrow{t^o}3Fe+4CO_2\uparrow\)
Đặt \(n_{CO\left(p/ứ\right)}=a\left(mol\right)=n_{CO_2}\) \(\Rightarrow n_{CO\left(dư\right)}=0,2-a\)
\(\Rightarrow\dfrac{44a+28\left(0,2-a\right)}{a+\left(0,2-a\right)}=20,4\cdot2\) \(\Rightarrow a=n_{CO\left(p/ứ\right)}=0,16\left(mol\right)\)
\(\Rightarrow n_{Fe_3O_4}=0,04\left(mol\right)\) \(\Rightarrow m_{Fe_3O_4}=0,04\cdot232=9,28\left(g\right)\)

Đáp án A
Hướng dẫn
Sơ đồ phản ứng :
0 , 02 m o l C 2 H 2 0 , 03 m o l H 2 → N i , t 0 hỗn hợp khí Y C 2 H 2 d ư C 2 H 4 C 2 H 6 H 2 → + d d B r 2 d ư hh khí Z C 2 H 6 H 2 d ư
Ta có: nhh Z = 0 , 28 22 , 4 = 0,0125 mol
M - Z = 10,08.2 = 20,16 => m hh Z = 0,0125 . 10,08 = 0,252 g
Áp dụng định luật bảo toàn khối lượng ta có:
mhh Y = m C 2 H 2 + m H 2 = 0,02.26 + 0,03.2 = 0,58 g
Dựa vào sơ đồ ta thấy: khối lượng bình brom tăng chính là khối lượnghi drocacbon không no được hấp thụ vào nên ta có:
∆ m d d B r 2 t ă n g = 0,58 – 0,252 = 0,328g
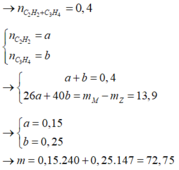
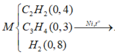
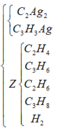
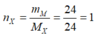
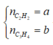
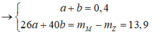
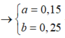
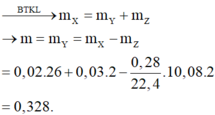
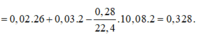
gọi số mol CO phảnứng là a mol suy ra số mol C02 tạo ra cũng là a mol
ta có (0,5-a)*28+44a=1.457*0,5*28 suy ra a=0,4 mol
suy ra số mol Fe304 là 0,1
m=23,2 gam
Mkhisp=28.1,457=40,796
=>sau phản ứng hỗn hợp khí gồm CO2; CO dư
do phản ứng xảy ra hoàn toàn,CO dư =>Fe3O4 hết chuyển thành Fe
PTHH 4CO+Fe3O4− − − (t∗) − − − >4CO2+3Fe
bđ:----0,5----------------------------------------(mol)
pứ:----x-----------x/4------------------x---------(mol)
sau:--(0,5-x)------x/4--------------------x----(mol)
áp dụng pp đưòng chéo ta có
\(\frac{nCO_2}{nCOdu}=\frac{4}{1}\\ hay:\frac{x}{0,5-x}=4\)
→ \(x=0,4\Rightarrow m=\left(0,\frac{4}{4}\right).232=23,2\left(g\right)\)
→ Đáp án D