Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Sắt từ oxit (Fe3O4)
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
- Axit Photphoric (H3PO4)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
- Canxi hidroxit (Ca(OH)2)
\(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)

\(2H_2O\underrightarrow{\text{diện phân}}2H_2+O_2\\ S+O_2\underrightarrow{t^o}SO_2\\ 2SO_2+O_2\xrightarrow[V_2O_5]{t^o}2SO_3\\ SO_3+H_2O\rightarrow H_2SO_4\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\\ Fe_3O_4A+4H_2\underrightarrow{t^o}3Fe+4H_2O\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
2Na + 2H2O -> 2NaOH + H2
S+O2 -t-> SO2
SO2 + O2 -> SO3
SO3 + H2O -> H2SO4
Fe3O4 + 4H2 -t-> 3Fe +4 H2O
Fe + H2SO4 -> FeSO4 + H2

a)
2H2O-đp>2H2+O2
b) SO4 ??
c)
2KClO3-to>2KCl+3O2
S+O2-to>SO2
SO2+O2-to, V2O5>SO3
SO3+H2O->H2SO4
2Cu+O2-to>2CuO
CuO+H2SO4->CuSO4+H2O
d) KClO3 + 6HCl → 3Cl2 + KCl + 3H2O
Cl2+Cu-to>CuCl2
2H2O -> (điện phân) 2H2 + O2
2KClO3 -> (t°, MnO2) 2KCl + 3O2
S + O2 -> (t°) SO2
2SO2 + O2 -> (t°, V2O5) 2SO3
SO3 + H2O -> H2SO4
Cu + H2SO4 (đặc nóng) -> CuSO4 + H2
2Cu + O2 -> (t°) 2CuO
CuO + 2HCl -> CuCl2 + H2O

Điều chế $NaOH$ :
$Na + H_2O \to NaOH + \dfrac{1}{2}H_2$
Điều chế $H_2SO_4$
$2H_2O \xrightarrow{điện\ phân} 2H_2 + O_2$
$S + O_2 \xrightarrow{t^o} SO_2$
$2SO_2 + O_2 \xrightarrow{t^o} 2SO_3$
$SO_3 + H_2O \to H_2SO_4$
Điều chế $FeSO_4$ :
$Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe +3 H_2O$
$Fe + H_2SO_4 \to FeSO_4 + H_2$

Cho Al tác dụng với dung dịch HCl:
2Al + 6HCl -> 2AlCl3 + 3H2
Cho H2 khử hỗn hợp oxit:
Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
CuO + H2 -> (t°) Cu + H2O
Thả hỗn hợp kim loại vào dung dịch HCl:
Fe + 2HCl -> FeCl2 + H2
Cứ không phản ứng
Lọc lấy Cu tinh khiết.
- Hòa tan hh vào dd HCl dư, thu đc dd gồm CuCl2, FeCl3, HCldư:
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
- Thêm tiếp Al dư vào dd, thu được hh rắn gồm Cu, Fe, Aldư:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(2Al+3CuCl_2\rightarrow2AlCl_3+3Cu\)
\(Al+FeCl_3\rightarrow AlCl_3+Fe\)
- Hòa tan hh rắn vào dd HCl dư, chất rắn không tan là Cu
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)

a) 2KClO3 -> 2KCl + 3O2
b) MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
b) SGK

\(KClO_3\xrightarrow[MnO_2]{t^o}KCl+\dfrac{3}{2}O_2\uparrow\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(2Al+3CuCl_2\rightarrow2AlCl_3+3Cu\)
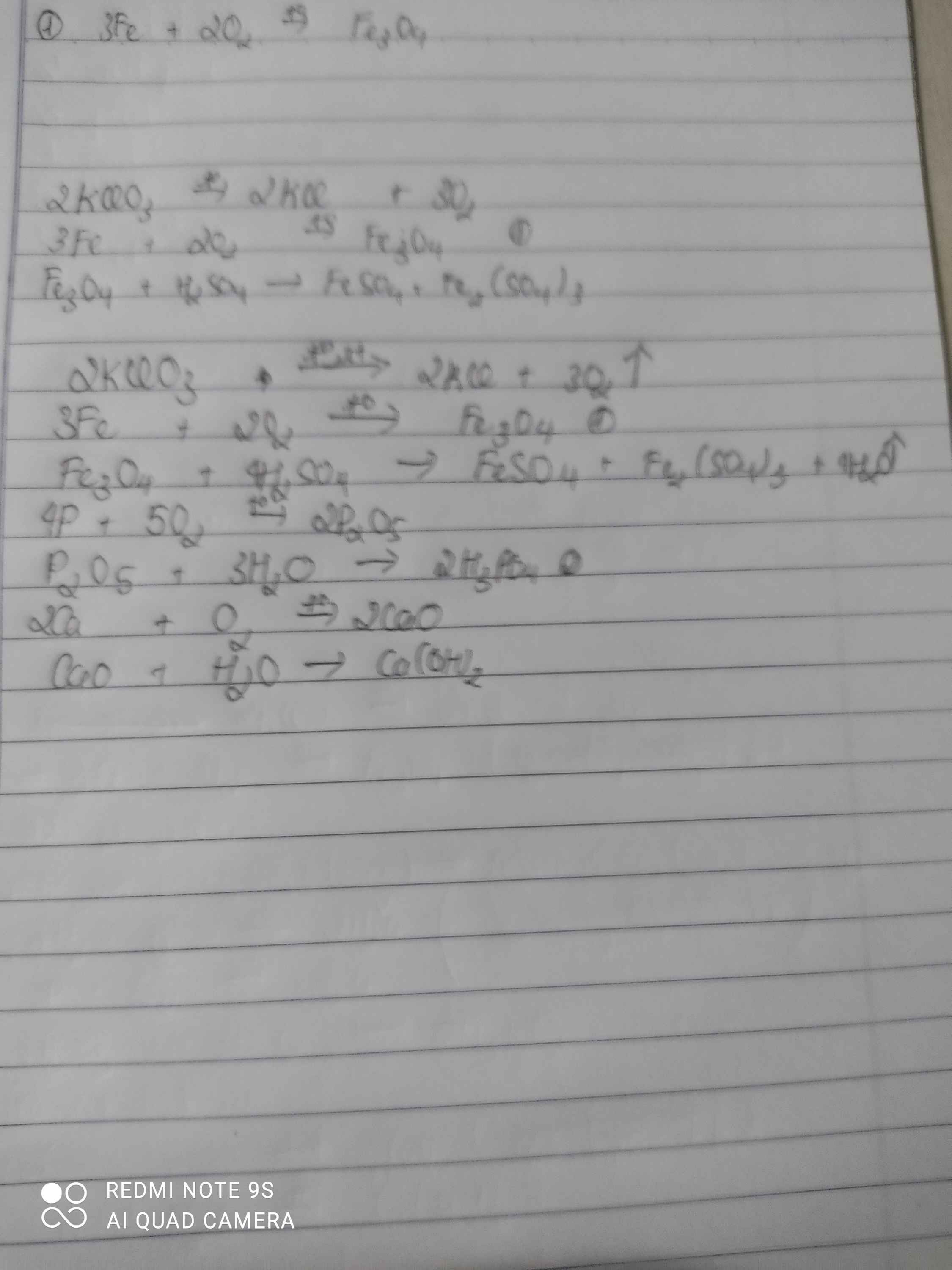
\(2KClO_3 \xrightarrow{t^o} 2KCl +3O_2\\ KClO_3 +6 HCl \to KCl + 3Cl_2 + 3H_2O\\ FeS + 2HCl \to FeCl_2 + H_2S\\ 4FeS + 7O_2 \xrightarrow{t^o} 2Fe_2O_3 + 4SO_2\)