Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nCu = 0,1
TN1: nH+ = 0,12
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O (1)
0,045 ← 0,12 → 0,03 (mol) ⇒ Cu dư
TN2: nH+ = 0,24
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O (2)
0,09 ←0,24 → 0,06 ⇒ Cu dư
Vậy nNO/(2) = 2nNO/(1) ⇒ 2a =b
Đáp án B.

Suy luận:
3Cu+ 8H++ 2NO3- → 3Cu2++ 2NO + 4 H2O
TN1: 4V1 ← V1 lít
TN2: 8V1 ← 2V1 lít
Nhận thấy: nH+ (TN2)= 2nH+ (TN1) → (1) là KNO3; (2) là HNO3; (3) là H2SO4
3Cu+ 8H++ 2NO3- → 3Cu2++ 2NO + 4 H2O
TN1: ban đầu 5.10-3 10.10-3
Phản ứng 5.10-3 1,25.10-3
TN3: ban đầu 15.10-3 5.10-3
Phản ứng 15.10-3 3,75.10-3
Các thể tích khí đo ở cùng điều kiện nên nNO(TN3)= 3nNO (TN1) → VNO(TN3)= 3VNO (TN1) hay V2= 3 V1
Đáp án B

Đây chỉ là một bài toán về kim loại Cu tác dụng với dung dịch có chứa NO3- và H+ đơn giản.
Để giải quyết bài này ta chỉ cần sử dụng đến phương trình ion thu gọn để giải quyết.
Thí nghiệm 1: ta có:
![]()
Xét phản ứng: 3Cu + 2NO3- + 8H+ → 3 C u 2 + +2NO + 4 H 2 O
Ban đầu: 0,12 (mol) 0,16 0,16
Phản ứng: 0,06 0,04 0,16 0,04
Sau phản ứng: 0,06 0,12 0 0,04
Thí nghiệm 2: ta có:
![]()
Xét phản ứng: 3Cu + 2 N O - 3 + 8 H + → 3 C u 2 + + 2NO + 4 H 2 O
Ban đầu: 0,12 (mol) 0,16 0,32
Phản ứng: 0,12 0,08 0,32 0,08
Sau phản ứng: 0 0,08 0 0,08
Ta thấy:
![]()
Đáp án C.

Quy đổi hỗn hợp Fe(a), O(b)
->56a+16b=17.2
mmuối =56a+62(2b+0,1.3)=57.4
->a=0.25,b=0.2
Dễ thấy 2a<2b+0,1.3<3a nên muối chưa Fe 2+ và Fe3+
->HNO3 hết
BT e: 2a+2nCu=2b+0,1.3
->nCu=0,1

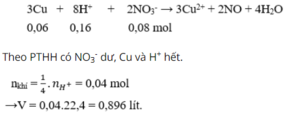

(*) TN1 :
3Cu + 8HNO3® 3Cu(NO3)2 + 2NO + H2O
0,06 0,08 ® 0,02 mol
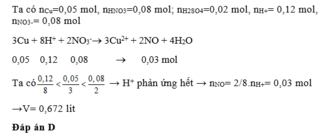
(*) TN2 :
3Cu + 8H+ + 2NO3-® 3Cu2+ + 2NO + 4H2O
0,06 0,16 0,08 ® 0,04 mol
→ b= 2a
Đáp án B