Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo đề, ta có: \(n_{X_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTTH: \(X_2+Cu\rightarrow CuX_2\)
Số mol: 0,05 ----------> 0,05
Theo phương trình, có: \(n_{CuX_2}=n_{Cu}=0,05\left(mol\right)\)
Hay: \(\dfrac{11,2}{64+X.2}=0,05\Leftrightarrow X=80\)
Vậy X là Brom.
Chon (B)

\(X_2+Mg\rightarrow MgX_2\)
0,1__________0,1
\(n_{X2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(M_{MgX2}=\frac{9,5}{0,1}=95\)
\(\Rightarrow X=35,5\left(Cl\right)\)

1/
gọi kim loại cần tìm là A
ta có: nH2= \(\dfrac{2,24}{22,4}\)= 0,1( mol)
PTPU
2A+ 2HCl\(\rightarrow\) 2ACl+ H2\(\uparrow\)
0,2.............................0,1... mol
\(\Rightarrow\) MA. 0,2= 7,8
\(\Rightarrow\) MA= \(\dfrac{7,8}{0,2}\)= 39( g/mol)
vậy kim loại cần tìm là kali( K)
mk chắc v
2/
gọi kim loại cần tìm là R
ta có: nH2= \(\dfrac{3,36}{22,4}\)= 0,15( mol)
PTPU
2R+ 2H2O\(\rightarrow\) 2ROH+ H2\(\uparrow\)
0,3...............................0,15.. mol
\(\Rightarrow\) 0,3.MR= 6,9
\(\Rightarrow\) MR= \(\dfrac{6,9}{0,3}\)= 23( g/mol)
vậy kim loại cần tìm là natri( Na)

X2+2M→2MX
x mol 2x2x mol
Khối lượng hợp chất A:2x(M+X)=4,12(1)
3X2+2Al→2AlX3
x mol 2x\3 mol
Khối lượng hợp chất B:2x3(27+3X)=3,56(2)
2M+S→M2S2
2x mol x mol
Khối lượng hợp chất C:x(2M+32)=1,56(3)
Giải hệ phương trình gồm 33 phương trình (1),(2),(3) tìm được x=0,02;X=80;M=23
do đó X là brom (Br=80);M(Br=80);
M là natri (Na=23)(Na=23).
Chất A là NaBr, B là AlBr3, C là Na2S

1.
Gọi CT chung của 2 kim loại là M
M + 2HCl --> MCl2 + H2 (1)
MCl2 +2AgNO3 --> M(NO3)2 + 2AgCl (2)
nM=\(\dfrac{8,8}{M_M}\)(mol)
theo (1) : nAgNO3=2nM=\(\dfrac{17,6}{M_M}\left(mol\right)\)
Khi thêm 0,5 mol AgNO3 thì không kết tủa hết , còn khi thêm 0,7 mol AgNO3 vào dd D thì AgNO3 dư
=> 0,5 < \(\dfrac{17,6}{M_M}\)< 0,7 => 25,14 < MM<35,2
=> 2 kim loại lần lượt là Na và K
2.
a) Gọi CT chung của 2 muối natri của 2 halogen là NaX
NaX + AgNO3 --> NaNO3 + AgX (1)
nNaX=\(\dfrac{22}{23+M_X}\)(mol)
nAgX=\(\dfrac{47,5}{108+M_X}\)(mol)
Theo (1) :nNaX=nAgX => \(\dfrac{22}{23+M_X}=\dfrac{47,5}{108+M_X}\)
=> MX=50,33(g/mol)
=> 2 halogen là : Cl2 và Br2
b) Gía sử có x mol NaCl
y mol NaBr
=> \(\left\{{}\begin{matrix}58,5x+103y=22\\143,5x+188y=47,5\end{matrix}\right.=>\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
=> mNaCl=11,7(g)
mNaBr=10,3(g)

- Gọi công thức của muối barihalogennua là BaR2 .
PTHH : \(BaR_2+H_2SO_4\rightarrow BaSO_4+2HR\)
- Gỉa sử số mol vừa đủ H2SO4 là 1 mol .
- Theo PTHH : \(n_{BaR_2}=n_{H_2SO_4}=n_{BaSO_4}=1\left(mol\right)\)
- Theo PTHH : \(n_{HR}=2n_{H_2SO_4}=2\left(mol\right)\)
\(m_{H_2SO_4}=n.M=1.98=98\left(g\right)\)
\(m_{ddH_2SO_4}=\frac{m_{H_2SO_4}.100\%}{C\%_{H_2SO_4}}=\frac{98.100\%}{5\%}=1960\left(g\right)\)
\(m_{BaR_2}=n.M=1.\left(137+2M_R\right)=137+2M_R\left(g\right)\)
\(m_{BaSO_4}=n.M=1.\left(137+32+16.4\right)=233\left(g\right)\)
- Ta có : \(m_{dd}=m_{H_2SO_4}+m_{BaR_2}-m_{BaSO_4}\)
=> \(m_{dd}=137+2M_R-233+1960=1864+2M_R\)
\(m_{HR}=n.M=2.M_{HR}=2.\left(M_R+1\right)\left(g\right)\)
Mà \(C\%_{HR}=\frac{m_{HR}}{m_{dd}}.100\%=3,77\%\)
=> \(\frac{2M_R+2}{1864-2M_R}=\frac{3,77}{100}\)
=> \(M_R\approx35,5\) ( đvc )
Vậy tên của halogen là clo .
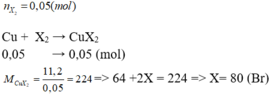
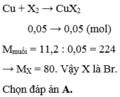
\(n_{X_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: \(Cu+X_2->CuX_2\)
Theo PT ta có: \(n_{CuX_2}=n_{X_2}=0,05\left(mol\right)\)
=> \(M_{CuX_2}=\dfrac{11,2}{0,05}=224\left(g/mol\right)\)
=> Ta có: \(64+2.X=224\)
\(\Leftrightarrow2X=160\Leftrightarrow X=80\left(Br\right)\)
Vậy nguyên tố halogen đó là Brom (Br)
X2 + Cu → CuX2
\(n_{X_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Theo PT: \(n_{CuX_2}=n_{X_2}=0,05\left(mol\right)\)
\(\Rightarrow M_{CuX_2}=\dfrac{11,2}{0,05}=224\left(g\right)\)
\(\Leftrightarrow64+2M_X=224\)
\(\Leftrightarrow2M_X=160\)
\(\Leftrightarrow M_X=80\left(g\right)\)
Vậy X là nguyên tố Brom