Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

KH nguyến tố halogen là X , đặt a là số mol ptu X2
ptpu:
Mg + X2 ----> MgX2
mol : a−−>a
2Al + 3X2 ---> 2AlX3
mol: a−−−>\(\frac{2a}{3}\)
từ pt => (24 + 2X).a =19 => a=\(\frac{19}{24+2X}\)
(27 + 3X).1,5a =17,8 => a= \(\frac{17,8.3}{\left(27+3X\right).2}\) =>X=35,5
![]()

Gọi số mol X2 là x mol
\(X_2+2M\rightarrow2MX\)
Ta có: \(n_{MX}=2n_{X2}=2x\left(mol\right)\Rightarrow2x\left(M+X\right)=8,24\)
\(3X_2+2Al\rightarrow2AlX_3\)
Ta có: \(n_{AlX3}=\frac{2}{3}n_{X2}=\frac{2x}{3}\rightarrow\frac{2x}{3}.\left(27+3X\right)=7,12\)
\(n_M=2n_{X2}=2x\left(mol\right)\)
\(2M+S\rightarrow M_2S\)
Ta có: \(n_{M2S}=\frac{1}{2}n_M=x\left(mol\right)\)
\(\rightarrow x\left(2M+32\right)=3,12\)
Giải phương trình 3 ẩn gồm xM, xX và x
Được xM=0,46; xX=1,6 và x=0,02 \(\rightarrow\) M=23; X=80 \(\rightarrow\) M là Na; X là Br
\(\rightarrow m=m_{Br2}=0,02.160=3,2\left(g\right)\)

a) Phương trình hóa học của phản ứng: Gọi X là kí hiệu nguyên tử khối của halogen.
Mg + X2 → MgX2
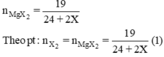
2Al + 3X2 → 2AlX3.
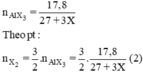
Cho (1) = (2). Giải ta rút ra X = 35,5 (Cl)
b) Thay X = 35,5 vào (1) ⇒ nCl2 = 0,2 mol ⇒ mCl2 = 14,2g.

a) Phương trình hóa học của phản ứng: Gọi X là kí hiệu nguyên tử khối của halogen.
2Al + 3X2 \(\rightarrow\) 2AlX3.
nAlX3 = 17,8/(27+3X).
nX2 = 3.17,8/ 2(27+3X). (1)
Mg + X2 \(\rightarrow\)MgX2
nMgX2 = 19 /(24 + 2X).
nX2 = 19/ (24+ 2X) (2).
Cho (1) = (2). Giải ta rút ra X = 35,5 (Cl)
b) mCl2 = 14,2g.
a) Phương trình hóa học của phản ứng: Gọi X là kí hiệu nguyên tử khối của halogen.
2Al + 3X2 →→ 2AlX3.
nAlX3 = 17,8/(27+3X).
nX2 = 3.17,8/ 2(27+3X). (1)
Mg + X2 →→MgX2
nMgX2 = 19 /(24 + 2X).
nX2 = 19/ (24+ 2X) (2).
Cho (1) = (2). Giải ta rút ra X = 35,5 (Cl)
b) mCl2 = 14,2g.

a)
$M + 2HCl \to MCl_2 + H_2$
$n_{HCl} = 0,3.1 = 0,3(mol)$
Theo PTHH : $n_M = \dfrac{1}{2}n_{HCl} = 0,15(mol)$
$\Rightarrow M = \dfrac{3,6}{0,15} = 24(Mg)$
b)
$n_{MgCl_2} = n_{Mg} = 0,15(mol)$
$m_{MgCl_2} = 0,15.95 = 14,25(gam)$
c) $n_{H_2} = n_{Mg} = 0,15(mol)$
$V_{H_2} = 0,15.22,4 = 3,36(lít)$



X2+2M→2MX
x mol 2x2x mol
Khối lượng hợp chất A:2x(M+X)=4,12(1)
3X2+2Al→2AlX3
x mol 2x\3 mol
Khối lượng hợp chất B:2x3(27+3X)=3,56(2)
2M+S→M2S2
2x mol x mol
Khối lượng hợp chất C:x(2M+32)=1,56(3)
Giải hệ phương trình gồm 33 phương trình (1),(2),(3) tìm được x=0,02;X=80;M=23
do đó X là brom (Br=80);M(Br=80);
M là natri (Na=23)(Na=23).
Chất A là NaBr, B là AlBr3, C là Na2S