Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: 2 MS + (2+n/2) O2 → M2On + 2 SO2
a 0,5 a ( n là hóa trị cao nhất của M trong muối)
M2On + 2nHNO3 → 2M(NO3)n + nH2O
0,5a an a
Khối lượng dung dịch HNO3 là 63.an.100/ 37,8 = 500an/3 (g)
Khối lượng dung dịch sau phản ứng: aM + 8an + 500an/3.
Nồng độ muối: (aM + 62an) : (aM + 524an/3) = 0,4172.
→ M = 18,65.n → Với n=3, M=56 (Fe) là thỏa mãn.
Ta có a(M + 32) = 4,4 → a = 0,05 (mol)
Khối lượng Fe(NO3)3 = 0,05. 242 = 12,1 (g)
Khối lượng dung dịch sau khi muối kết tinh tách ra: aM + 524an/3 – 8,08 = 20,92 (g)
Khối lượng Fe(NO3)3 còn lại trong dung dịch: 20,92.34,7/100= 7,26 (g)
Khối lượng muối Fe(NO3)3 kết tinh là: 12,1-7,26 = 4,84.
Đặt công thức muối: Fe(NO3)3.mH2O → (4,84 : 242) . (242 + 18m) = 8,08 → m=9
Vậy công thức của muối kết tinh là : Fe(NO3)3.9H2O.

\(2MS+\left(2+\dfrac{n}{2}\right)O_2\rightarrow M_2O_n+2SO2\)(n hóa trị cao nhất của M)
x-----------------------------0,5x
\(M_2O_n+2nHNO_3\rightarrow2M\left(NO_3\right)_n+nH_2O\)
0,5x---------xn-------------2x
Khối lượng dung dịch là :\(\dfrac{63\cdot xn}{0,378}+xM+8an=\dfrac{524xn}{3}+aM\left(g\right)\)
Nồng độ muối \(\dfrac{x\left(M+62n\right)}{xM+\dfrac{524nx}{3}}=0,4127\Rightarrow M=18,65n\)
Thay n= 1 ; 2 ;3 vào M=18,65n
Nhận thấy n=3 , M=56(Fe) (thõa mãn)
---> x=0,05(mol) n=3
\(m_{Fe\left(NO_3\right)_3}=0,05\cdot242=12,1\left(g\right)\)
khối lượng dd sau khi muốn kết tinh táh ra :
\(0,025\cdot160+25-8,8=20,92\left(g\right)\)
Sau khi muối kết tih tách ra dd muối còn 34,7% => muối dư
hay \(m_{Fe\left(NO3\right)_3}dư\)
khối lương muối dư là : 0,347.20,92=7,26(g)
LƯợng muối đi kết tinh là:\(12,1-7,6=4,48\left(g\right)\)

Gọi x là số mol của MS
\(MS+O_2\underrightarrow{t^o}M+SO_2\uparrow\)
x -----------> x
\(M+H_2SO_4\rightarrow MSO_4+H_2\)
x ----> x -----------> x -------->
\(mdd_{H_2SO_4}=\dfrac{98x.100}{36,75}=266,67x\)
\(C\%_{MSO_4}=\dfrac{xM+96x}{xM+266,67x-2x}.100=41,67\%\)
\(\Leftrightarrow\dfrac{M+96}{M+264,67}.100=41,67\%\)
M = 24 => Mg
cthc: MgS

1 Gọi công thức oxit của kim loại hóa trị III là A2O3,ta có các phương trình sau
A2O3+3H2SO4--->A2(SO4)3+3H2O (1)
0,02 0,06 0,02
Vì sau phản ứng (1) dung dịch còn có thể phản ứng với CaCO3 giải phóng khí CO2=>axit H2SO4 dư,ta có phương trình
H2SO4+CaCO3--->CaSO4+CO2+H2O (2)
0,01 0,01 0,01 0,01
nCO2=0,224:22,4=0,01 mol
Khối lượng muối A2(SO4)3 sau khi cô cạn là
9,36-0,01x(40+96)=8 g
Ta thấy rằng A2O3=3,2 g,sau phản ứng tạo thành muối A2(SO4)3=8g Như vậy khối lượng tăng thêm là do 3 gốc -SO4 thay thế cho 3 nguyên tử Oxi,vậy khối lượng tăng thêm là 8-3,2 =4,8 g
nA2SO4=4,8:(96x3-16x3)=0,02 mol
=>khối lượng muối=0,02x(2xR+96x3)=8
=>R=56
R hóa trị III, có M=56=>R là Fe,công thức oxit là Fe2O3
nH2SO4=0,01+0,06=0,07 mol
mH2SO4=0,07x98=6,86g
C% dd H2SO4=(6,86:200)x100%=3,43%
2.
a/ Khí B: H2nH2O = 0.25 mol => nH2 = 0.25 mol
=> nH2/ B = 0.5 mol => nH+ = 1 mol = nHCl pứ = nCl- ( H+ + Cl- = HCl )
=> mCl- = 35.5g => m muối A = 35.5 + 18.4 = 53.9g
b/ m ( dd NaOH ) = 240g => m NaOH = 48g => n NaOH = 1.2 mol
H2 + Cl2 ---> 2HCl
0.5 1
NaOH + HCl --> NaCl + H2O
1 1 1 1
Khối lượng dd lúc này: 1*36.5 + 240 = 276.5 gam
mNaCl tạo thành = 58.5g => C% NaCl = 21.15%
%NaOH dư = ( 1.2 - 1 ) * 40 / 276.5 = 2.89%
c/ Gọi khối lượng mol của KL nhẹ hơn ( A ) là x => khối lượng mol của KL còn lại ( B ) là 2.4 * x
Vì số mol của 2 KL bằng nhau và bằng a mol
=> 3a + 2a = 5a = 1 mol => a = 0.2 mol ( KL hóa trị III td với 3 mol HCl, KL hóa trị II td 2 mol HCl )
=> 0.2*x + 0.2*2.4*x = 18.4 => x = 27.
A: Al
B: Zn
Anh giải đặt ẩn nhiều,trông hơi khó coi nên em trình bày cho đẹp nha!!Bài 2 còn 1 cách giải đấy em tự tìm tham khảo nha!!Chúc em học tốt!!

PT: \(MO+H_2SO_4\rightarrow MSO_4+H_2O\)
Ta có: \(n_{MO}=\dfrac{10}{M_M+16}\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{MSO_4}=n_{MO}=\dfrac{10}{M_M+16}\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=\dfrac{10}{M_M+16}.98=\dfrac{980}{M_M+16}\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{\dfrac{980}{M_M+16}}{24,5\%}=\dfrac{4000}{M_M+16}\left(g\right)\)
⇒ m dd A = \(10+\dfrac{4000}{M_M+16}\left(g\right)\)
\(\Rightarrow C\%_{MSO_4}=\dfrac{\left(M_M+96\right).\dfrac{10}{M_M+16}}{10+\dfrac{4000}{M_M+16}}.100\%=33,33\%\)
\(\Rightarrow M_M=64\left(g/mol\right)\)
Vậy: M là Cu.
Ta có: \(n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)=n_{CuSO_4\left(A\right)}\)
m dd A = 60 (g) ⇒ m dd B = 60 - 15,625 = 44,375 (g)
\(\Rightarrow n_{CuSO_4\left(B\right)}=\dfrac{44,375.\dfrac{1600}{71}\%}{160}=0,0625\left(mol\right)\)
BTNT Cu, có: \(n_{CuSO_4.nH_2O\left(C\right)}=0,125-0,0625=0,0625\left(mol\right)\)
\(\Rightarrow M_C=\dfrac{15,625}{0,0625}=250\left(g/mol\right)\Rightarrow n=\dfrac{250-160}{18}=5\)
Vậy: C là CuSO4.5H2O
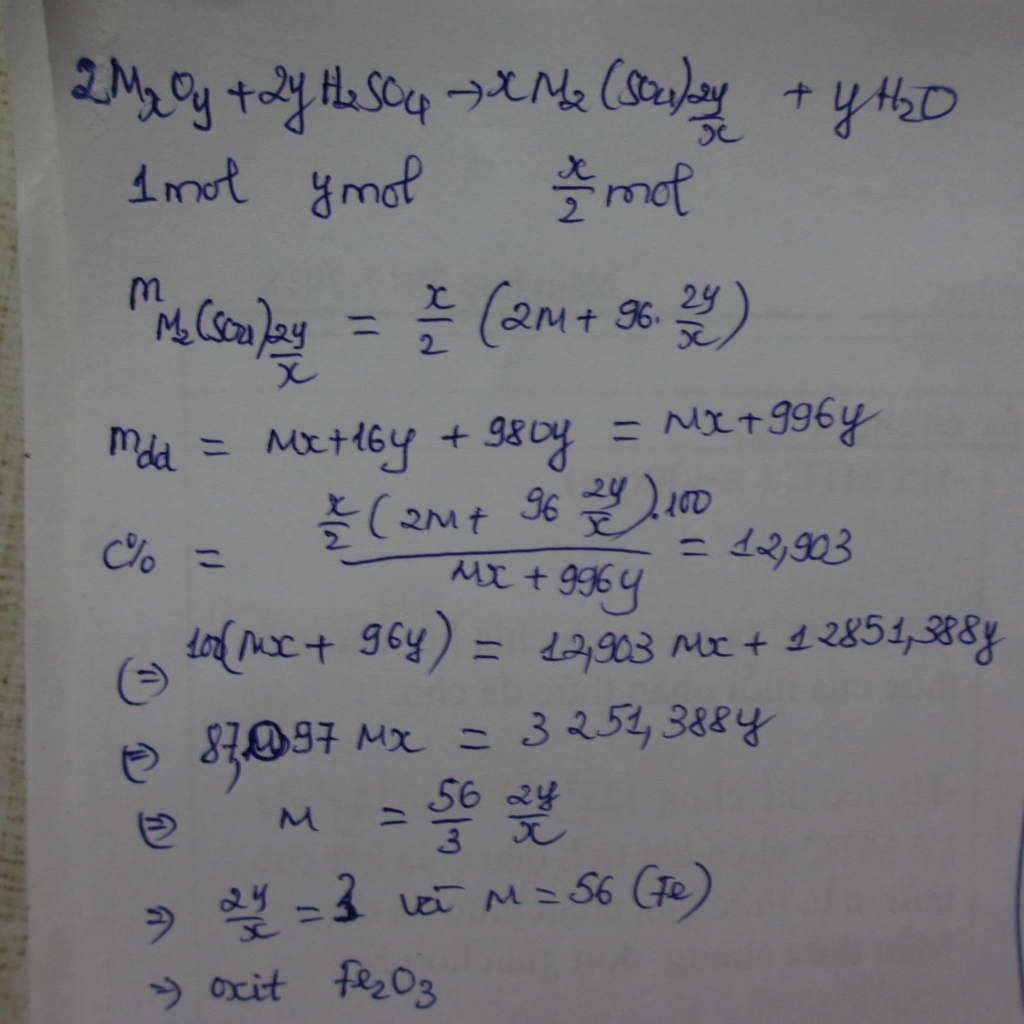
muối sunfua k phải sunfat
thế còn đáp án