Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(2MS+\left(2+\dfrac{n}{2}\right)O_2\rightarrow M_2O_n+2SO2\)(n hóa trị cao nhất của M)
x-----------------------------0,5x
\(M_2O_n+2nHNO_3\rightarrow2M\left(NO_3\right)_n+nH_2O\)
0,5x---------xn-------------2x
Khối lượng dung dịch là :\(\dfrac{63\cdot xn}{0,378}+xM+8an=\dfrac{524xn}{3}+aM\left(g\right)\)
Nồng độ muối \(\dfrac{x\left(M+62n\right)}{xM+\dfrac{524nx}{3}}=0,4127\Rightarrow M=18,65n\)
Thay n= 1 ; 2 ;3 vào M=18,65n
Nhận thấy n=3 , M=56(Fe) (thõa mãn)
---> x=0,05(mol) n=3
\(m_{Fe\left(NO_3\right)_3}=0,05\cdot242=12,1\left(g\right)\)
khối lượng dd sau khi muốn kết tinh táh ra :
\(0,025\cdot160+25-8,8=20,92\left(g\right)\)
Sau khi muối kết tih tách ra dd muối còn 34,7% => muối dư
hay \(m_{Fe\left(NO3\right)_3}dư\)
khối lương muối dư là : 0,347.20,92=7,26(g)
LƯợng muối đi kết tinh là:\(12,1-7,6=4,48\left(g\right)\)

Gọi x là số mol của MS
\(MS+O_2\underrightarrow{t^o}M+SO_2\uparrow\)
x -----------> x
\(M+H_2SO_4\rightarrow MSO_4+H_2\)
x ----> x -----------> x -------->
\(mdd_{H_2SO_4}=\dfrac{98x.100}{36,75}=266,67x\)
\(C\%_{MSO_4}=\dfrac{xM+96x}{xM+266,67x-2x}.100=41,67\%\)
\(\Leftrightarrow\dfrac{M+96}{M+264,67}.100=41,67\%\)
M = 24 => Mg
cthc: MgS

Gọi m_ddH2SO4 = 294 gam → nH2SO4 =0,6 mol
R2O3 + 3H2SO4 → R2(SO4)3 +3H2O
0,2 0,6 0,2 0,6
=> m = 294 + 9,6 + 0,4R
=> 0,2(2R + 96.3)/303,6 + 0,4R = 0,21756
=> R = 27 => R = AI

Đặt CT muối cacbonat: MCO3
Giả sử có 1 mol MCO3 phản ứng
MCO3 + H2SO4 ===> MSO4 + CO2 + H2O
1 1 1 1 1 ( mol)
<=>(M + 60) 98 (M + 96) 44 ( gam)
mdung dịch ( sau pứ)= M + 60 + 90 x 100 / 20 - 44 = ( M + 506 ) gam
Ta có: M + 96 = 0,28196 x ( M+506) => M = 65
=> M là Zn
Vậy công thức của muối cacbonat: ZnCO3
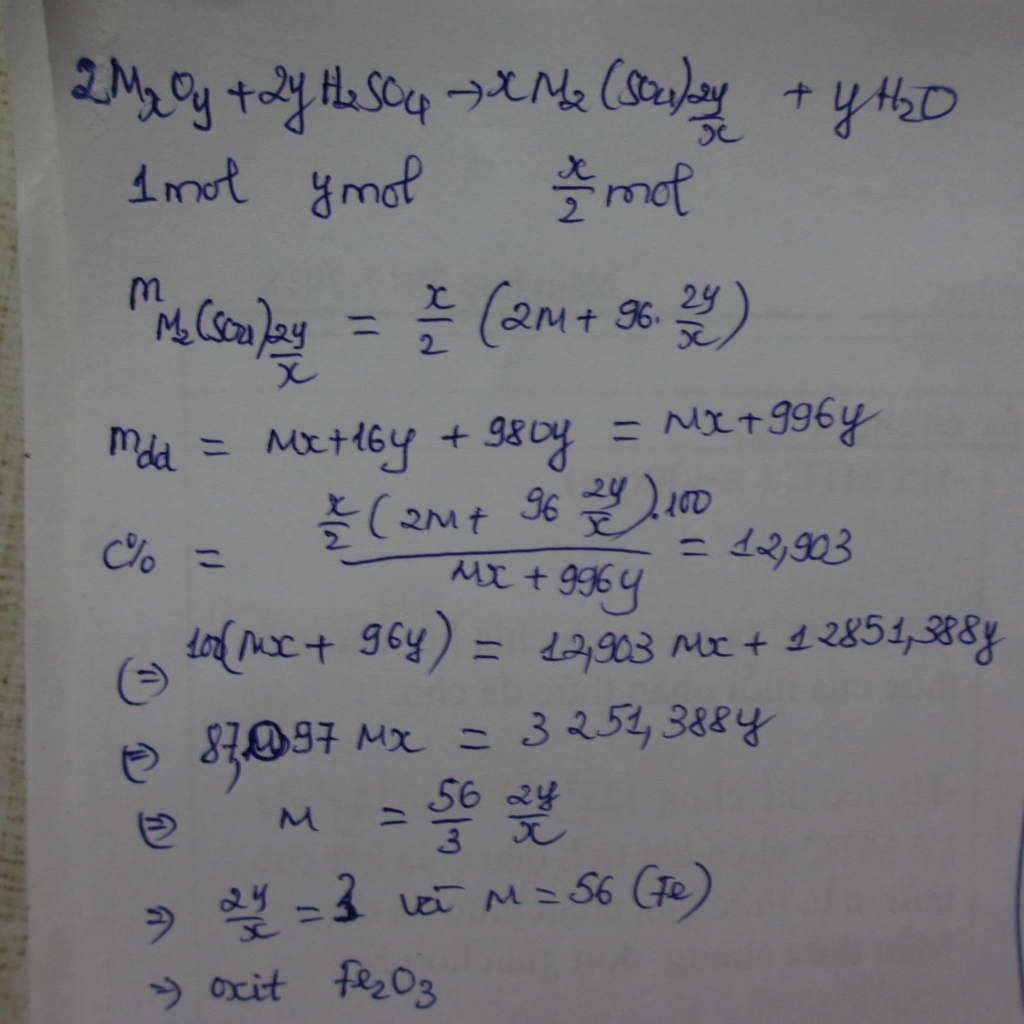
PTHH: 2 MS + (2+n/2) O2 → M2On + 2 SO2
a 0,5 a ( n là hóa trị cao nhất của M trong muối)
M2On + 2nHNO3 → 2M(NO3)n + nH2O
0,5a an a
Khối lượng dung dịch HNO3 là 63.an.100/ 37,8 = 500an/3 (g)
Khối lượng dung dịch sau phản ứng: aM + 8an + 500an/3.
Nồng độ muối: (aM + 62an) : (aM + 524an/3) = 0,4172.
→ M = 18,65.n → Với n=3, M=56 (Fe) là thỏa mãn.
Ta có a(M + 32) = 4,4 → a = 0,05 (mol)
Khối lượng Fe(NO3)3 = 0,05. 242 = 12,1 (g)
Khối lượng dung dịch sau khi muối kết tinh tách ra: aM + 524an/3 – 8,08 = 20,92 (g)
Khối lượng Fe(NO3)3 còn lại trong dung dịch: 20,92.34,7/100= 7,26 (g)
Khối lượng muối Fe(NO3)3 kết tinh là: 12,1-7,26 = 4,84.
Đặt công thức muối: Fe(NO3)3.mH2O → (4,84 : 242) . (242 + 18m) = 8,08 → m=9
Vậy công thức của muối kết tinh là : Fe(NO3)3.9H2O.