Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

_ \(d^{hhkhi}/H_2=9,66\Rightarrow\overline{M}_{hhkhi}=19,32\)
Tính đc tỉ lệ: \(\dfrac{n_{CO}}{n_{H_2}}=2\Rightarrow n_{CO}=2n_{H_2}\) (1)
PTHH: \(3H_2+Fe_2O_3\rightarrow2Fe+3H_2O\)
\(3CO+Fe_2O_3\rightarrow2Fe+3CO_2\)
Gọi a,b lần lượt là số mol của H2, CO
Từ (1) => -2a + b = 0
\(\dfrac{2}{3}a+\dfrac{2}{3}b=0,3\) => a = 0,15; b = 0,3
\(\Rightarrow V_{H_2}=0,15.22,4=3,36l\)
\(V_{CO}=6,72l\).

\(n_{CO\left(dư\right)}=a\left(mol\right)\)
\(n_{CO_2}=b\left(mol\right)\)
\(n_B=a+b=0.5\left(mol\right)\left(1\right)\)
\(m_B=2\cdot20.4\cdot0.5=20.4\left(g\right)\)
\(\Rightarrow28a+44b=20.4\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.4\)
\(n_{CO\left(pư\right)}=n_{CO_2}=0.4\left(mol\right)\)
\(BTKL:\)
\(m_X+m_{CO}=m_A+m_B\)
\(\Leftrightarrow m_X=64+0.4\cdot44-0.4\cdot28=70.4\left(g\right)\)
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam.

Gọi số mol H2 trong hỗn hợp A là x, số mol CO là y. Ta có:
\(\frac{2x+28y}{2\left(x+y\right)}=9,66\Rightarrow\frac{x}{y}=\frac{1}{2}\)
PTHH: \(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\left(1\right)\)
\(Fe_2O_3+3CO\rightarrow3CO_2+2Fe\left(2\right)\)
Gọi số mol của H2 tham gia phản ứng là a mol
\(\Rightarrow n_{CO}\) tham gia phản ứng là 2a
Theo pt (1): \(n_{Fe}=\frac{2a}{3}\)
Theo pt (2): \(n_{Fe}=\frac{4a}{3}\)
\(\Rightarrow n_{Fe}\) do 2 phản ứng tạo thành: \(\frac{2a}{3}+\frac{4a}{3}=2a=\frac{16,8}{56}=0,3\Rightarrow a=0,15\)
\(\Rightarrow V_{h^2A}=\left(0,15+0,3\right).22,4=10,08\left(l\right)\)

- Đặt \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\Rightarrow27a+24b=10,2\left(1\right)\)
Khí thu được sau p/ứ là khí H2: \(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
2 3 (mol)
a 3/2 a (mol)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
1 1 (mol)
b b (mol)
Từ hai PTHH trên ta có: \(\dfrac{3}{2}a+b=0,5\left(2\right)\)
\(\left(1\right),\left(2\right)\) ta có hệ: \(\left\{{}\begin{matrix}27a+24b=10,2\\\dfrac{3}{2}a+b=0,5\end{matrix}\right.\)
Giải ra ta có \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\)
a) \(\%Al=\dfrac{m_{Al}}{m_{hh}}.100\%=\dfrac{0,2.27}{10,2}.100\%\approx52,94\%\)
\(\%Mg=100\%-\%Al=100\%-52,94=47,06\%\)
b)
\(3H_2+Fe_2O_3\rightarrow^{t^0}2Fe+3H_2O\)
3 1 2 (mol)
0,5 1/6 1/3 (mol)
\(m_{Fe}=\dfrac{1}{3}.56=\dfrac{56}{3}\left(g\right)\)
\(m_{Fe_2O_3\left(pứ\right)}=\dfrac{1}{6}.160=\dfrac{80}{3}\left(g\right)\)
\(m_{Fe_2O_3\left(dư\right)}=60-m_{Fe}=60-\dfrac{56}{3}=\dfrac{124}{3}\left(g\right)\)
\(a=\dfrac{124}{3}+\dfrac{80}{3}=68\left(g\right)\)

a) Ta có: nH2=4,48/22,4=0,2(mol)
PTHH: Fe +2 HCl -> FeCl2 + H2
0,2________0,4______0,2__0,2(mol)
mFe=0,2.56=11,2(g)
=> %mFe= (11,2/17,6).100=63,636%
=> %mCu= 36,364%
b) Fe2O3 + 3 H2 -to-> 2 Fe + 3 H2O
Ta có: nH2=0,2(mol) => nFe=2/3. 0,2= 2/15(mol)
=> mFe= 2/15 . 56=7,467(g)
Số moll của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : Fe + 2HCl → FeCl2 + H2\(|\)
1 2 1 1
0,2 0,2
a) Số mol của sắt
nFe = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Khối lượng của sắt
mFe = nFe . MFe
= 0,2. 56
= 11,2 (g)
Khối lượng của đồng
mCu = 17,6 - 11,2
= 6,4 (g)
0/0Fe = \(\dfrac{m_{Fe}.100}{m_{hh}}=\dfrac{11,2.100}{17,6}=63,64\)0/0
0/0Cu = \(\dfrac{m_C.100}{m_{hh}}=\dfrac{6,4.100}{17,6}=36,36\)0/0
b) 3H2 + Fe2O3 → (to) 2Fe + 3H2O\(|\)
3 1 2 3
0,2 0,13
Số mol của sắt
nFe = \(\dfrac{0,2.2}{3}=0,13\left(mol\right)\)
Khối lượng của sắt
mFe = nFe . MFe
= 0,13 . 56
= 7,28 (g)
Chúc bạn học tốt

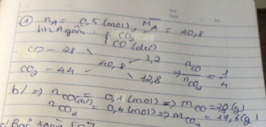
Gọi nH2 : xmol
nCO: y mol
d(H2,CO)/H2=9,66
\(\rightarrow\)M(H2,CO)=19,32
=>nH2:nCO2=0,5
=> nH2=0,5nCO2=>x=0,5y=>x-0,5y=0(1)
Fe2O3 + 3H2 \(\rightarrow\)2Fe + 3H2O
________ x_____2/3x
Fe2O3 + 3CO \(\rightarrow\) 2Fe + 3CO2
y_____2/3y
nFe=16,8/56=0,3
2/3x+2/3y=0,3(2)
(1)(2)\(\rightarrow\)x=0,15 ; y=0,3
V A=0,45.22,4=10,08lit
Fe2O3 + 3H2 -to-> 2Fe + 3H2O
Fe2O3 + 3CO -to-> 2Fe + 3CO2
=> nA = 3/2 nFe = 0.45 mol
=> V = 0.45*22.4 = 10.08 l