Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
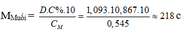
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
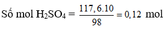
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%

\(n_{HCl}=\dfrac{200\cdot7.3\%}{36.5}=0.4\left(mol\right)\)
\(M+2HCl\rightarrow MCl_2+H_2\)
\(0.2.....0.4.........0.2........0.2\)
\(m_{MCl_2}=0.2\cdot\left(M+71\right)\left(g\right)\)
\(m_{dd}=0.2M+200-0.2\cdot2=0.2M+199.6\left(g\right)\)
\(C\%MCl_2=\dfrac{0.2\cdot\left(M+71\right)}{0.2M+199.6}\cdot100\%=12.05\%\)
\(\Rightarrow M=56\)
\(M:Sắt\)


BTKL: mD + mNaHCO3 = mCO2 + mE
mD + 179,88 = 44.0,2 + 492 => mD = 320,92
BTKL: mMg + mddHCl = mH2 + mD
=> 24 . 0,4 + mddHCl = 2 . 0,4 + 320,92 => mddHCl = 312,12
=> C%HCl = 11,69%

1/ PT : X + 2H2O -> X[OH]2 + H2
mol : \(\frac{6}{M_X}\) -> \(\frac{6}{M_X}\)
=> mH2 = \(\frac{12}{M_X}\) => mdd = m+6 - \(\frac{12}{M_X}\)
Ta có: m+5,7 = m+6 - \(\frac{12}{M_X}\)
<=> \(\frac{12}{M_X}\)= 0,3 => MX = 40 => X là Canxi [Ca]
2/ Dặt nHCl= a [a> 0] => mddHCl= 36,5a : 14,6 x 100= 250a
PT : X + 2HCL => XCl2 + H2
mol : a/2 a -> a/2 a/2
mH2 = a/2 x 2 = a ; mX = a/2 . MX
m XCl2= a/2 x [MX +71]
mdd XCL2= a/2 .MX + 250a - a = a/2 .MX +249a
Ta có :\(\frac{\frac{a}{2}\times M_X+\frac{71}{2}a}{M_X\times a:2+249a}\times100\%=24,15\%\)
<=> \(\frac{M_X+71}{M_X+498}=24,15\%\Leftrightarrow M_X=65\)=> X là kẽm [Zn]

Đặt a,b là số mol Mg, R trong 8 gam A. Đặt x,y là hoá trị thấp cao của R
mA = 24a + bR = 8 (1)
Với HCl -> 2a + bx = 0,2 .2 (2)
Trong 9,6 gam A ( gấp 1,2 lần 8 gam A ) chứa 1,2a và 1,2b mol Mg, R
Với Cl2 -> 2 . 1,2a + 1,2by = 2 ( 30,9 - 9,6 ) / 71 (3)
Với 1 ≤ x ≤ y ≤ 3 -> Chọn x = 2; y = 3
(2)(3) -> a = b = 0,1
(1) -> R= 56 -> = Fe

PTHH :
R + Cl2 -^t0-> RCl2
0,1mol.............0,1mol
R + 2HCl -> RCl2 + H2
0,1mol...0,2mol
=> MRCl2 = \(\dfrac{13,6}{0,1}=136\) => MR = 136 - 71 = 65(g)
=> R là Zn
R + Cl2 \(^{to}\rightarrow\)RCl2
0,1 .............→0,1
R + 2 HCl → RCl2 + H2 \(\uparrow\)
0,1←0,2
nHCl = 1. 0,2 = 0,2 mol
- ta có :
mRCl2 = nRCl2 . MRCl2
⇒ MRCl2 = \(\dfrac{13,6}{0,1}\) =136
⇔ 136 = R + 35,5.2
⇒ R = 65 (Zn)
- vậy R là kẽm (Zn)

Kim loại cần tìm đặt là A.
=> CTHH oxit: A2O3
\(A_2O_3+H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3H_2O\\ m_{ddsau}=10,2+331,8=342\left(g\right)\\ m_{A_2\left(SO_4\right)_3}=\dfrac{342}{100}.10=34,2\left(g\right)\\ n_{oxit}=\dfrac{34,2-10,2}{96.3-16.3}=0,1\left(mol\right)\\ M_{A_2O_3}=\dfrac{10,2}{0,1}=102\left(\dfrac{g}{mol}\right)=2M_A+48\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_A=\dfrac{102-48}{2}=27\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Nhôm\left(Al=27\right)\\ \Rightarrow CTHH.oxit:Al_2O_3\)


R + Cl2 → RCl2
R + 2HCl → RCl2 + H2
nHCl = 0,2.1 = 0,2 mol => nR = 0,2/2 = 0,1 mol
Mà nRCl2 = nR
=> MRCl2 = \(\dfrac{13,6}{0,1}\)= 136 (g/mol) => MR = 136 - 35,5.2 = 64 g/mol
Vậy R là kim loại đồng (Cu)