Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
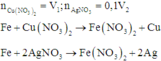
Vì khối lượng chất rắn thu được ở hai thí nghiệm bằng nhau nên khối lượng chất rắn tăng lên ở hai thí nghiệm bằng nhau.
Khi đó
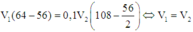

Đáp án C
Giả sử m = 10 g, khi đó n(X) = 0,1 mol
Theo dữ kiện đề bài thì khi cho Y vào nước dư thu được 0,025 mol CaCO3
→ hỗn hợp X chứa 0,025 mol CaCO3 và 0,075 mol KHCO3. Các quá trình phản ứng xảy ra:
2KHCO3 → K2CO3 + CO2
CaCO3 → CaO + CO2
Khi cho Y vào nước dư thì:
K2CO3 + CaO + H2O → CaCO3 + 2KOH
Vậy dung dịch E gồm K2CO3 dư (0,0125) và KOH (0,05)
PT:
H+ + OH- → H2O
H+ + CO32- → HCO3-
H+ + HCO3- → CO2 + H2O
Lượng HCl cho vào E đến khi bắt đầu thoát khí là:
n(HCl)1 = n(K2CO3) + n(KOH) = 0,0625
Lượng HCl cho vào E đến khi thoát hết khí là:
n(HCl)2 = 2n(K2CO3) + n(KOH) = 0,075
=> n(HCl)1 : n(HCl)2 = 5:6

* Tìm thành phần của các dung dịch đánh số:
Ta có phản ứng hòa tan kim loại Cu:

![]()
Mặt khác, quan sát hai thí nghiệm thứ nhất và thứ hai ta thấy: ở thí nghiệm thứ hai lượng khí NO thu được gấp đôi lượng khí NO ở thí nghiệm thứ nhất, hai thí nghiệm này sử dụng chung dung dịch (1) và khác nhau ở dung dịch (2) hay dung dịch (3).
Nên dung dịch (1) là KNO3, dung dịch (2) là HNO3 và dung dịch (3) là H2SO4.
* Tìm mối quan hệ giữa V1 và V2:
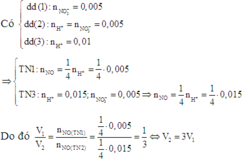
Đáp án C.

Đáp án C
Dễ dàng suy ra được (1) KNO3; (2) HNO3; (3) H2SO4
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
(1) và (2) Bđ 1 2
Pư 1 0,25 0,25
(2) và (3) Bđ 3 1
Pư 3 0,75 0,75
=> V2 = 3V1
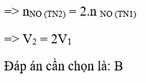



Đáp án D
nH+ (1) = nH+ (2) ⇒ 4V1 = V2 (3+1.2) ⇒V1 = 1,25V2