Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Fe + 4HNO3 -> Fe(NO3)3 + NO + 2H2O (1)
Al2O3 + 6HNO3 -> 2Al(NO3)3 + 3H2O (2)
nNO=0,1(mol)
Theo PTHH 1 ta có:
nFe=nNO=0,1(mol)
mFe=56.0,1=5,6(g)
%mFe=\(\dfrac{5,6}{15,8}.100\%=35,443\%\)
%mAl2O3=100-35,443=64,557%
b;
nAl2O3=\(\dfrac{15,8-5,6}{102}=0,1\left(mol\right)\)
Theo PTHH 1 ta có:
nHNO3(1)=4nFe=0,4(mol)
nFe(NO3)3=nFe=0,1(mol)
Theo PTHH 2 ta có:
nHNO3(2)=6nAl2O3=0,6(mol)
nAl(NO3)3=2nAl2O3=0,2(mol)
Vdd HNO3=\(\dfrac{0,4+0,6}{2}=0,5\left(lít\right)\)
CM dd Fe(NO3)3=\(\dfrac{0,1}{0,5}=0,2M\)
CM dd Al(NO3)3=\(\dfrac{0,2}{0,5}=0,4M\)
ko phải thầy đâu,em mới lớp 9 thua cả chị đấy,gọi là em dc rồi
Nguyễn Kiều Trang

\(n_{NO}=\dfrac{0,672}{22,4}=0,03mol\)
\(\Rightarrow n_{HNO_3}=4n_{NO}=4\cdot0,03=0,12mol\)
\(\Rightarrow n_{NO_3^-}=0,12mol\)
\(m_{muối}=m_{kl}+62n_{NO_3^-}=5,68+62\cdot0,12=13,12g\)
\(n_{NO}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Quy đổi hỗn hợp X về Fe (x mol) và O (y mol)
Ta có: mX = mFe + mO → 56x + 16y = 5,68 (1)
Các quá trình trao đổi electron:
\(\overset{0}{Fe}\rightarrow\overset{+3}{Fe}+3e\)
\(\overset{0}{O}+2e\rightarrow\overset{-2}{O}\)
\(\overset{+5}{N}+3e\rightarrow\overset{+2}{N}\)
Áp dụng bảo toàn electron: \(3n_{Fe}=2n_O+3n_{NO}\)
\(\Rightarrow3x=2y+3.0,03\rightarrow3x-2y=0,09\left(2\right)\)
Từ (1) và (2) → x = 0,08; y = 0,075
Bảo toàn nguyên tố Fe:
\(nFe\left(NO_3\right)_3=n_{Fe}=0,08\left(mol\right)\)
→ m muối = 0,08.242 = 19,36 gam

Coi như hỗn hợp gồm Fe, FeO, Fe2O3, Fe3O4 gồm có x mol Fe và y mol O
Ta có 56x+16y= 11,36 (1)
Ta có nNO= 0,06 mol
QT cho e :
Fe → Fe3++ 3e
x 3x mol
QT nhận e :
O+ 2e→ O-2
y 2y mol
N+5+ 3e → NO
0,18←0,06
Theo ĐL BT electron thì : ne cho= ne nhận nên 3x= 2y+ 0,18 (2)
Từ (1) và (2) ta có x= 0,16 và y= 0,15
Bảo toàn nguyên tố Fe có nFe(NO3)3= nFe= x= 0,16 mol→ mFe(NO3)3=38,72 gam
Đáp án D

Đáp án B
♦ CB1: 0,6 mol CO + O → 0,225 mol CO + 0,375 mol CO2.
||→ nO trong Y = nO trong X – nO bị CO lấy
= 0,2539m ÷ 16 – 0,375 mol.
♦ CB3: BT e kiểu "mới":
∑nNO3– trong muối KL = 3nNO + 2nO trong Y
= 0,2539m ÷ 8 + 0,69 mol.
||→ mmuối = mKL + mNO3–
= 0,7461m + 62 × (0,2539m ÷ 8 + 0,69) = 5,184m
Giải phương trình → yêu cầu giá trị của m ≈ 17,320 gam

Đáp án C
Z gồm CO và CO2
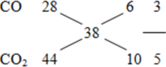
⇒nCO = 0,15 mol ;
n
C
O
2
= 0,25 mol
⇒ nO bị chiếm = 0,25 mol
⇒ nO còn lại = 0,2539m/16−0,25 mol
nNO = 7,168/22,4 = 0,32 mol
Coi hỗn hợp Y gồm kim loại: 0,7461m (gam) và O: 0,2539m/16−0,25 (mol)
Ta có:
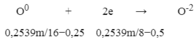
O0 + 2e → O-2
0,2539m/16−0,25 0,2539m/8−0,5
N+5 + 3e → N+2
0,96 0,32
⇒ m muối = m KL +
m
N
O
3
-
trong muối
= 0,7461m + 62. (0,2539m/8−0,5+0,96)
⇒ 3,456m = 2,714m + 28,52
⇔ m = 38,45 gam

- Viết đúng ptpư:
\(Fe+4HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\)
\(3Cu+8HNO_3\rightarrow2Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(nNO=0,04\left(mol\right)\)
Gọi nFe là x(mol) ; nCu là y(mol)
ta có hệ pt:
\(\left\{{}\begin{matrix}m_{hh}=56x+64y=3,04\\nNO=x+\dfrac{2}{3y}=0,04\end{matrix}\right.\)
Giải hệ ta được: x = 0,02 mol ; y = 0,03 mol
\(\Rightarrow mFe=0,02.56=1,12\left(g\right)\)
\(mCu=0,03.64=1,92\left(g\right)\)

Quy đổi hỗn hợp Fe(a), O(b)
->56a+16b=17.2
mmuối =56a+62(2b+0,1.3)=57.4
->a=0.25,b=0.2
Dễ thấy 2a<2b+0,1.3<3a nên muối chưa Fe 2+ và Fe3+
->HNO3 hết
BT e: 2a+2nCu=2b+0,1.3
->nCu=0,1
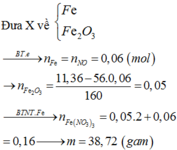
Theo đề bài ta có : \(\left\{{}\begin{matrix}nNO=\dfrac{0,224}{22,4}=0,01\left(mol\right)\\nHNo3=\dfrac{33.21}{100.63}=0,11\left(mol\right)\end{matrix}\right.\)
PTHH :
(1) \(Fe+4HNO3->Fe\left(NO3\right)3+NO\uparrow+H2O\)
0,01mol...0,04mol....................................0,01mol
(2) \(Fe2O3+6HNO3->2Fe\left(NO3\right)3+3H2O\)
a) khối lượng của Fe và Fe2O3 trong hỗn hợp ban đầu là : \(\left\{{}\begin{matrix}mFe=0,01.56=0,56\left(g\right)\left(g\right)\\mFe2O3=2,16-0,56=1,6\left(g\right)\end{matrix}\right.\)
b) nồng độ % các chất trong dung dịch sau phản ứng là :
Theo PTHH 2 ta có : nFe(NO3)2 = 2nFe2O3 =2 \(\dfrac{1,6}{160}=0,02\left(mol\right)\)
=> C%\(_{\text{dd}Fe\left(NO3\right)3}=\dfrac{\left(0,01+0,02\right).242}{2,16+33-0,01.30}.100\%\approx20,83\%\)
Vậy...
bài này làm tương tự thôi ạ,có gì đâu