Cho 16 gam CUO vào 200ml dung dịch HNO3 được dung dịch x . Cho x tác dụng với dung dịch NaOH 1M đến khi phản ứng hoàn toàn thấy hết 500ml. tính nồng độ mol của dung dịch HNO3?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


X+ HNO3→ Dung dịch Y
Dung dịch Y + NaOH→ Khí
→Dung dịch Y phải có NH4NO3
NH4NO3+ NaOH → NaNO3+ NH3↑ + H2O
0,01← 0,01 mol
QT nhận e:
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (3)
0,1 0,01 mol
nHNO3= nH+= 0,1 mol →CM HNO3= 0,1/0,2= 0,5 (M)
Đáp án C

a, \(n_{HNO_3}=0,3.1=0,3\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,1.1=0,1\left(mol\right)\)
PT: \(2HNO_3+Ba\left(OH\right)_2\rightarrow Ba\left(NO_3\right)_2+2H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{2}>\dfrac{0,1}{1}\), ta được HNO3 dư.
Theo PT: \(\left\{{}\begin{matrix}n_{Ba\left(NO_3\right)_2}=n_{Ba\left(OH\right)_2}=0,1\left(mol\right)\\n_{HNO_3\left(pư\right)}=2n_{Ba\left(OH\right)_2}=0,2\left(mol\right)\end{matrix}\right.\)
⇒ nHNO3 (dư) = 0,3 - 0,2 = 0,1 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{Ba\left(NO_3\right)_2}}=\dfrac{0,1}{0,3+0,1}=0,25\left(M\right)\\C_{M_{HNO_3\left(dư\right)}}=\dfrac{0,1}{0,3+0,1}=0,25\left(M\right)\end{matrix}\right.\)
b, Ta có: \(n_{Na_2CO_3}=0,25.0,5=0,125\left(mol\right)\)
PT: \(Na_2CO_3+2HNO_3\rightarrow2NaNO_3+CO_2+H_2O\)
______0,05______0,1_______________0,05 (mol)
⇒ VCO2 = 0,05.22,4 = 1,12 (l)
\(Na_2CO_3+Ba\left(NO_3\right)_2\rightarrow2NaNO_3+BaCO_{3\downarrow}\)
0,075________0,075_______________0,075 (mol)
⇒ mBaCO3 = 0,075.197 = 14,775 (g)

nCaCO3=8,4:(40+12+16.3)=0,084 mol
nH2SO4= 0,5.1=0,5 mol
PTHH: H2SO4+ CaCO3 --> CaSO4↓ + CO2 +H2O
theo đề: 0,5 mol: 0,084 mol
=> H2SO4 de theo CaCO3
phản ứng : 0,084mol<----0,084 mol---> 0,084mol
=> CM=\(\frac{0,084}{0,5}=0,168M\)

Đáp án A
Do Fe dư nên chỉ tạo ra Fe2+.
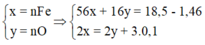
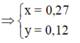
4H+ + NO3- + 3e → NO + 2H2O
2H+ + O + 2e → H2O
=> nHNO3 = nH+ = 4nNO + 2nO = 4.0,1 + 2.0,12 = 0,64
=> [HNO3] = 0,64/0,2 = 3,2M => Chọn A.

Nhận thấy, ở lần 1 thì chưa có kết tủa tan còn lần 2 đã có kết tủa tan (nếu ở trường hợp cả 2 lần đều có kết tủa tan thì chênh lệch số mol kết tủa sẽ bằng chênh lệch số mol NaOH cho vào)
Lần 2:


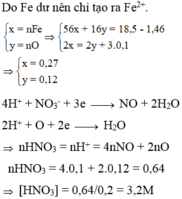



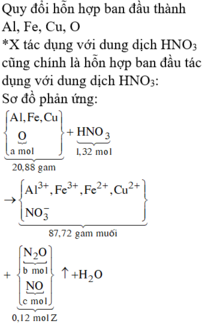
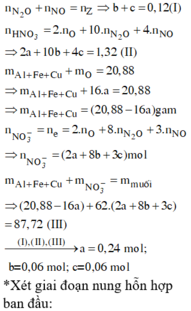
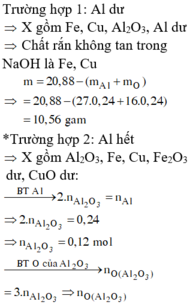
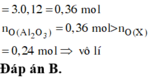

\(CuO+2HNO_3\rightarrow Cu\left(NO_3\right)_2+H_2O\)
0,2 0,4 0,2
Giả sử \(HNO_3\) không dư, phản ứng trên vừa đủ.
Dung dịch X chỉ chứa duy nhất \(Cu\left(NO_3\right)_2\)
\(Cu\left(NO_3\right)_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaNO_3\)
0,25<------0,5
\(n_{NaOH}=0,5.1=0,5\left(mol\right)\)
Từ phương trình hóa học thấy 0,25>0,2 => Giả sử sai, \(HNO_3\) dư sau phản ứng.
Đặt số mol \(HNO_3\) dư là x
\(HNO_3+NaOH\rightarrow NaNO_3+H_2O\)
x------->x
\(Cu\left(NO_3\right)_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaNO_3\)
0,2---------->0,4
Có: \(x+0,4=n_{NaOH}=0,5\Rightarrow x=0,1\)
=> Tổng mol \(HNO_3=0,4+x=0,4+0,1=0,5\left(mol\right)\)
\(\Rightarrow CM_{HNO_3}=\dfrac{0,5}{0,2}=2,5\left(M\right)\)