nêu khái niệm về thể tích mol của chất khí ở áp xuất 1 bar và 25 độ c
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Phương trình trạng thái khí lí tưởng: \(\dfrac{P.V}{T}=\text{const}\)
Suy ra: \(\dfrac{P_1.V_1}{T_1}=\dfrac{P_2.V_2}{T_2}\)
\(\Rightarrow T_2=\dfrac{P_2.V_2}{P_1.V_1}.T_1=\dfrac{7.10^5}{0,8.10^5.5}.(273+50)=565.25K\)
\(\Rightarrow t_2=565,25-273=292,25^0C\)

Đáp án: A
Ta có:
Thể tích của bình chứa là: V = 22,4 l = 22,4.10 − 3 m 3
Thể tích của một phân tử oxi bằng: V 0 = 4 3 π r 3
Thể tích riêng của các phân tử oxi bằng: V ' = N A V 0 = 4 3 π N A r 3
Xét tỉ số: V V ' = 22,4.10 − 3 4 3 π N A r 3 = 22,4.10 − 3 4 3 π .6,023.10 23 . 10 − 10 3 = 8,9.10 3
=> Thể tích riêng của các phân tử ôxi nhỏ hơn thể tích bình chứa 8,9.10 3 lần

Chọn B.
Vì quá trình biến đổi là đẳng nhiệt nên ta có:
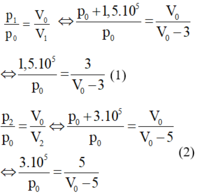
Từ (1) và (2), ta tìm được p 0 = 6 . 10 5 Pa; V 0 = 15 lít.

Chọn B.
Vì quá trình biến đổi là đẳng nhiệt nên ta có:
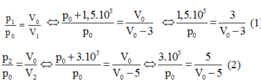
Từ (1) và (2), ta tìm được p0 = 6.105 Pa; V0 = 15 lít.

Chọn B.
Vì quá trình biến đổi là đẳng nhiệt nên ta có:
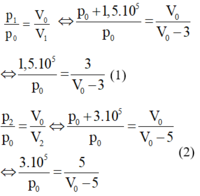
Từ (1) và (2), ta tìm được p0 = 6 . 10 5 Pa; V0 = 15 lít

Chọn A.
Thể tích của bình chứa là V = 22,4 ℓ = 22,4.10-3 m3.
Thể tích của 1 phân tử ôxi bằng V0 = .4/3 π r 3
Thể tích riêng của các phân tử ôxi bằng NAV0 = 4 3 π N A r 3
Thể tích riêng của các phân tử ôxi nhỏ hơn thể tích bình chứa


Công do chất khí thực hiện
A = p . Δ V = 1 , 5.10 5 .2.10 − 2 = 3000 J
Vì khí nhận nhiệt lượng và thực hiện công nên A<0
Theo nguyên lí I:
Q = Δ U − A = 4 , 28 − − 3000 = 3004 , 28 J
Đáp án: B
Thể tích mol của chất khí là thể tích chiếm bởi N nguyên tử hoặc phân tử của chất khí đó. Ở điều kiện chuẩn (áp suất 1 bar, nhiệt độ \(25^oC\)), thể tích mol của các chất khí đều bằng \(24,79l\).