Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ΔrH298
o = -890,3 kJ
Biết nhiệt tạo thành chuẩn của CO2(g) và H2O(l) tương ứng là –393,5 và –285,8 kJ/mol. Hãy tính
nhiệt tạo thành chuẩn của khí methane.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(C_2H_6+\dfrac{7}{2}O_2->2CO_2+3H_2O\\ \Delta_rH^o_{298}=2\left(-393,5\right)+3\left(-285,8\right)-\left(-84,7\right)\\ \Delta_rH^o_{298}=-1559,7kJ\)
Phương trình nhiệt hoá học thì không cần ghi điều kiện nhé.

Gọi nhiệt tạo thành chuẩn của khí methane là x
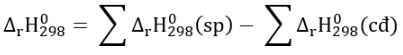
\(\rightarrow\) -890,3 = 2.(-285,8) -393,5 - x - 2.0
\(\rightarrow\) x = – 74,8 kJ/mol

nC2H2 = 1/26 (mol)
Đốt cháy 1/26 mol C2H2 tỏa ra 49,98 kJ
=> Đốt cháy 1 mol C2H2 tỏa ra x kJ
=> x = 1 x 49,98 : (1/26) = 1299,48 kJ
=> ${\Delta _r}H_{298}^0$ = -1299,48 kJ (vì đây là phản ứng tỏa nhiệt nên enthalpy mang giá trị âm)

\(\Delta_fH^o_{298}\left[CO_2\right]=-94,05\cdot4,184=-393,5052kJ\cdot mol^{-1}\\ \Delta_fH^o_{298}\left[CO\right]=\dfrac{-393,5052\cdot2-\left(-135,28\cdot4,184\right)}{2}=-110,5kJ\cdot mol^{-1}\)

\(N_2O_4+3CO->N_2O+3CO_2\\ \Delta_rH^o_{298}=82,05+3\left(-393,50\right)-\left(9,16+3\left(-110,50\right)\right)\\ \Delta_rH^o_{298}=-776,11kJ\)

Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{H_2}=y\end{matrix}\right.\)
\(n_{O_2}=\dfrac{7,437}{24,79}=0,3mol\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x 2x x 2x ( mol )
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
y 1/2 y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}2x+\dfrac{1}{2}y=0,3\\2x+y=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(m=m_{CH_4}+m_{H_2}=\left(0,1.16\right)+\left(0,2.2\right)=2g\)
\(V_{CO_2}=0,1.24,79=2,479l\)
\(\Delta_fH^{^{ }o}_{298}\left[CH_4\right]=-\left(-890,3-\left(-393,5\right)-\left(-285,8\right)\right)\\ \Delta_fH^{^{ }o}_{298}\left[CH_4\right]=211kJ\cdot mol^{-1}\)