khử 160g đồng ii oxit ( Cuo ) bằng khí h2 a)tính thể tích khí h2 tham gia phản ứng b) khối lượng cu sinh ra bao nhiêu gam c) tính khối lượng nước thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


CuO+H2-to>Cu+H2O
0,09----0,09---0,09
n CuO=\(\dfrac{7,2}{80}\)=0,09 mol
=>m Cu=0,09.64=5,76g
=>VH2=0,09.22,4=2,016l
\(n_{CuO}=\dfrac{7,2}{80}=0,09mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,09 0,09 0,09 ( mol )
\(m_{Cu}=0,09.64=5,76g\)
\(V_{H_2}=0,09.22,4=2,016l\)

hình như bn ghi sai r đó phải là:đồng oxit mới phải chứ![]()

\(n_{CuO}=\dfrac{80}{80}=1\left(mol\right)\)
Pt : \(CuO+H_2\underrightarrow{t^o}Cu+H_2O|\)
1 1 1 1
1 1 1
a) \(n_{Cu}=\dfrac{1.1}{1}=1\left(mol\right)\)
⇒ \(m_{Cu}=1.64=64\left(g\right)\)
b) \(n_{H2}=\dfrac{1.1}{1}=1\left(mol\right)\)
\(V_{H2\left(dktc\right)}=1.22,4=22,4\left(l\right)\)
Chúc bạn học tốt

a, \(FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
b, \(n_{FeO}=\dfrac{7,2}{72}=0,1\left(mol\right)\)
\(n_{Fe}=n_{FeO}=0,1\left(mol\right)\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
c, \(n_{H_2}=n_{FeO}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)

\(n_{CuO}=\dfrac{m}{M}=\dfrac{12}{64+16}=0,15\left(mol\right)\)
\(a,PTHH:CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(0,15:0,15:0,15\left(mol\right)\)
\(b,m_{Cu}=n.M=0,15.64=9,6\left(g\right)\)
\(c,V_{H_2}=n.22,4=0,15.22,4=3,36\left(l\right)\)

A. \(H_2+CuO\rightarrow Cu+H_2O\)
B. \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Cu}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,1.64=6,4\left(g\right)\)
C. Theo PTHH: \(n_{H_2}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)

a, \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,15\left(mol\right)\Rightarrow V_{H_2}=0,15.22,4=3,36\left(l\right)\)
b, Có lẽ đề hỏi bao nhiêu gam đồng thay vì "bao nhiêu gam sắt" bạn nhỉ?
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,25}{1}>\dfrac{0,15}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)\)
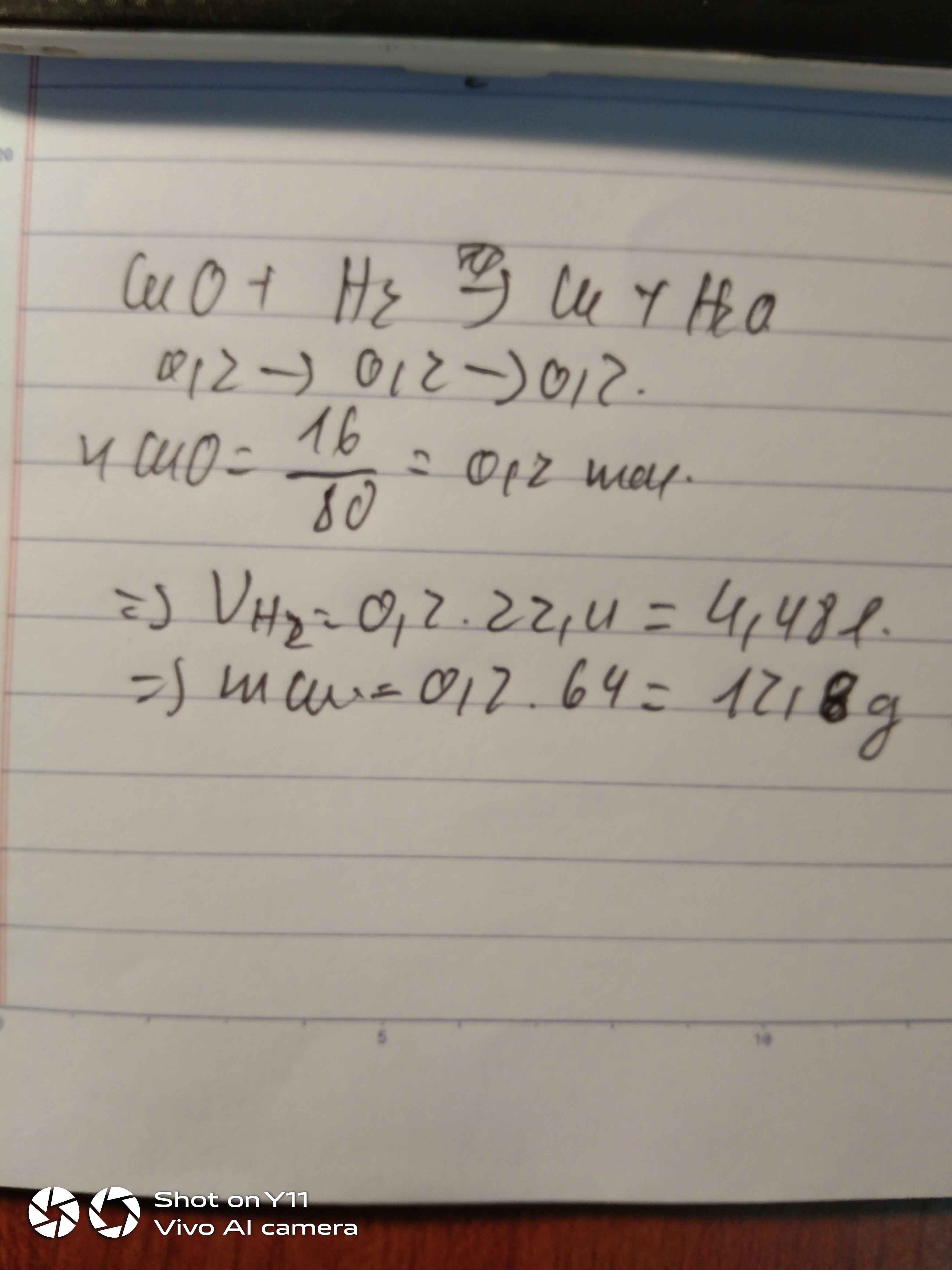
`CuO + H_2` $\xrightarrow[]{t^o}$ `Cu + H_2 O`
`2` `2` `2` `2` `(mol)`
`n_[CuO] = 160 / 80 = 2 (mol)`
`a) V_[H_2] = 2 . 22,4 = 44,8 (l)`
`b) m_[Cu] = 2 . 64 = 128 (g)`
`c) m_[H_2 O] = 2 . 18 = 36 (g)`