Để hòa tan hết m gam nhôm cần dung dịch chứa 29,4 gam H 2 SO 4 , thu được V lít H 2(đktc).a/ Tính m và V.b/ Dẫn lượng khí H 2 thu được ở trên đi qua ống sứ có chứa 28,8 gam FeO. Sau một thời gian,thấy khối lượng chất rắn trong ống còn 26,4 gam. Tính hiệu suất phản ứng khử FeO.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, nCO2 = 0,06 ( mol )
=> nCO = 0,06 ( mol )
ADĐLBTKL : \(m_{CO}+m_{Fe2O3}=m_{hh}+m_{CO_2}\)
=> \(m=m_{Fe2O3}=5,44+0,06.44-0,06.28=6,4\left(g\right)\)
b, nCO2 lấy = 0,012 ( mol )
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
.0,002........0,002........0,002...............
=> nCO2 còn lại = 0,012 - 0,002 = 0,01 ( mol )
\(Ca\left(OH\right)_2+2CO_2\rightarrow Ca\left(HCO_3\right)_2\)
......0,005.......0,01........0,005.......
\(Ca\left(HCO_3\right)_2\rightarrow CaCO_3+H_2O+CO_2\) ( * )
...0,005..............0,005................
=> Tổng nCa(OH)2 = 0,002 + 0,005 = 0,007 ( mol )
=> CMCa(OH)2 = 0,014M .
=> m1 = mCaCO3 (*) = 0,5 ( g )
Vậy ...

Đáp án A
Quy đổi hỗn hợp X gồm Fe và O
mX = 56nFe + 16nO = 10,44 (1)


Đáp án A.
→ n X = 0 , 5 ; n C O 2 = 0 , 15 ; n C O = 0 , 1 → n N 2 = 0 , 25
→
n
X
=
0
,
25
→
n
C
a
C
O
3
=
n
C
O
+
n
C
O
2
=
0
,
125
→
m
=
12
,
5

Đáp án A.
![]()
![]()
→ n X = 0 , 25 → n C a C O 3 = n C O + n C O 2 = 0 , 125 → m = 12 , 5
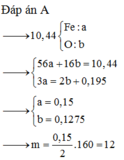


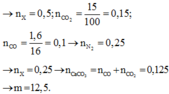
a)
\(n_{H_2SO_4} = \dfrac{29,4}{98} = 0,3(mol)\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\)
Theo PTHH :
\(n_{Al} = \dfrac{2}{3}n_{H_2SO_4} = 0,2(mol)\\ n_{H_2} = n_{H_2SO_4} = 0,3(mol)\)
Suy ra :
\(m = 0,2.27 = 5,4(gam)\\ V = 0,3.22,4 = 6,72(lít)\)
b)
\(FeO + H_2 \xrightarrow{t^o} Fe + H_2O\\ n_{FeO} = \dfrac{28,8}{72} = 0,4 > n_{H_2} = 0,3\)
Do đó,hiệu suất tính theo số mol của H2.
Gọi :\( n_{H_2O} = n_{H_2\ pư} = a(mol)\)
Bảo toàn khối lượng :
\(m_{FeO} + m_{H_2} = m_{chất\ rắn} + m_{H_2O}\\ \Leftrightarrow 28,8 + 2a = 26,4 + 18a\\ \Leftrightarrow a = 0,15(mol)\)
Vậy hiệu suất phản ứng : H = \(\dfrac{0,15}{0,3}.100\% = 50\%\)