Cho 100 ml dung dịch NaOH 3M tác dụng với 100 ml dung dịch AgCl3 2M. Kết thúc phản ứng, thu được m gam kết tủa. Giá trị của m là
A. 23,4
B. 7,8
C. 15,6
D. 3,9
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
n C O 3 2 - = 0,2 mol; n H C O 3 - = 0,3 mol.
→ tỉ lệ 2 : 3.
→ 2x và 3x là số mol CO32– và HCO32– đã phản ứng
→ n H + = 2x.2 + 3x = 0,42 => x = 0,06 → n C O 2 = 2x + 3x = 0,3 mol.
Có n O H - = 0,36
Xét tỉ lệ T = n O H - n C O 2 thấy tạo ra đồng thời 2 muối CO32– và HCO3–.
→ n C O 3 2 - = 0,06; n H C O 3 - = 0,24
n B a 2 + = 0,08 → n B a C O 3 = 0,06 → m B a C O 3 = 11,82 gam.

Chọn A.
n(CO32-) = 0,2 mol; n(HCO3-) = 0,3 mol.
→ tỉ lệ 2 : 3.
→ 2x và 3x là số mol CO32- và HCO32- đã phản ứng
→ n(H+) = 2x.2 + 3x = 0,42 => x = 0,06 → n(CO2) = 2x + 3x = 0,3 mol.
Có n(OH-) = 0,36
Xét tỉ lệ T = n(OH-) / n(CO2) thấy tạo ra đồng thời 2 muối CO32- và HCO3-.
→ n(CO32-) = 0,06; n(HCO3-) = 0,24
n(Ba2+) = 0,08 → n(BaCO3) = 0,06 → m(BaCO3) = 11,82 gam

Đáp án C
n(CO32–) = 0,2 mol; n(HCO3–) = 0,3 mol.
→ tỉ lệ 2 : 3.
→ 2x và 3x là số mol CO32– và HCO32– đã phản ứng
→ n(H+) = 2x.2 + 3x = 0,42 => x = 0,06 → n(CO2) = 2x + 3x = 0,3 mol.
Có n(OH–) = 0,36
Xét tỉ lệ T = n(OH–) / n(CO2) thấy tạo ra đồng thời 2 muối CO32– và HCO3–.
→ n(CO32–) = 0,06; n(HCO3–) = 0,24
n(Ba2+) = 0,08 → n(BaCO3) = 0,06 → m(BaCO3) = 11,82 gam.

Đáp án A
Trong 300 ml dung dịch X có m gam Al 2 SO 4 3 , suy ra trong 150 ml dung dịch X sẽ có 0,5m gam Al 2 SO 4 3 và có số mol là x.
Lượng Al 2 SO 4 3 phản ứng ở 2 thí nghiệm là như nhau. Lượng OH - ở TN2 nhiều hơn ở TN1, lượng kết tủa (y mol) ở TN2 ít hơn ở TN1 (2y mol). Chứng tỏ ở TN2 kết tủa Al OH 3 đã bị hòa tan một phần, ở TN1 kết tủa có thể bị hòa tan hoặc chưa bị hòa tan.
● Nếu ở TN1 kết tủa Al OH 3 chưa bị hòa tan, áp dụng bảo toàn điện tích trong các dung dịch sau phản ứng, ta có :
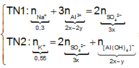
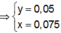
![]() thỏa mãn
thỏa mãn
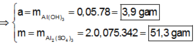
● Ở TN1 kết tủa Al OH 3 đã bị hòa tan, áp dụng bảo toàn điện tích cho dung dịch sau phản ứng, ta có:
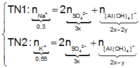
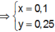
![]() (loại) (*)
(loại) (*)
PS : Nếu không sử dụng biểu thức (*) để biện luận loại trường hợp không thỏa mãn thì sẽ tính ra đáp án B. Nhưng đó là kết quả sai.

Nhận thấy khi lượng NaOH tăng lên, lượng AlCl3 không đổi thì lượng kết tủa tăng lên → thí nghiệm 1 thì NaOH hết, AlCl3 còn dư ; thí nghiệm 2 cả NaOH và AlCl3 đều hết (xảy ra hiện tượng hòa tan kết tủa)
Thí nghiệm 1: Ta có 3× nkết tủa = nOH- = 0,6 mol → 0,2a= 0,6 → a= 3
Thí nghiệm 2:Ta có 4×nAl3+ = nOH- + nkết tủa → 4×0,5b= 0,4×3 + 0,3 → b= 0,75
Đáp án A
⇒ m A l O H 3 = 7 , 8 g
=> Chọn đáp án B.