Dung dịch X có chứa: 0,07 mol Na+; 0,02 mol SO42- và x mol OH-. Dung dịch Y có chứa ClO4-, NO3- và y mol H+; tổng số mol ClO4- và NO3- là 0,04. Trộn X và Y được 100ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của H2O) là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
Bảo toàn điện tích đối với dung dịch X, ta có: 0,07.1 = 0,02.2 + x.1 → x = 0,03
Bảo toàn điện tích đối với dung dịch Y, ta có: y.1 = 0,04.1 ⇒ y = 0,04
Khi trộn dung dịch X và Y thì H+ + OH- → H2O
(0,04) (0,03)
⇒ nH+còn dư = 0,04 – 0,03 = 0,01 mol ⇒ [H+] còn dư = 0,01/0,1 = 0,1M ⇒ pH = – lg[H+] = 1

Đáp án A
Theo ĐL BT ĐT thì x = 0,03 mol
Theo ĐLBT ĐT thì nH+ = nClO4(-)+ nNO3(-) = 0,04 mol
H+ + OH- → H2O
0,04 0,03
nH+ dư = 0,01 mol; [H+] dư = 0,01/0,1 = 0,1 suy ra pH = 1

Mình nghĩ bạn chưa hiểu rõ vấn đề ban đầu nó :
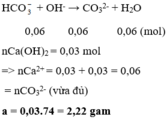
H+ +CO3 2- => HCO3-
Sau đó
HCO3 - + H+ => co2
Như vậy bài toán sẽ ra 0,01 mol co2 là đáp án C

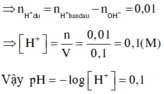
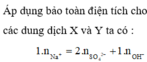





Bảo toàn điện tích đối với dung dịch X, ta có: 0,07.1 = 0,02.2 + x.1 → x = 0,03
Bảo toàn điện tích đối với dung dịch Y, ta có: y.1 = 0,04.1 → y = 0,04
Khi trộn dung dịch X và Y thì
H+ + OH- → H2O
(0,04) (0,03)
→ nH+còn dư = 0,04 – 0,03 = 0,01 mol → [H+] còn dư = 0,01/0,1 = 0,1M → pH = – lg[H+] = 1
Đáp án C