Hãy giải thích sự liên kết giữa hai nguyên tử H tạo thành phân tử H 2 giữa hai nguyên tử C1 tạo thành phân tử Cl 2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Nguyên tử Cl có 7 electron lớp ngoài cùng và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
Từ đây em tự vẽ khi mỗi nguyên tử góp 1e dùng chung

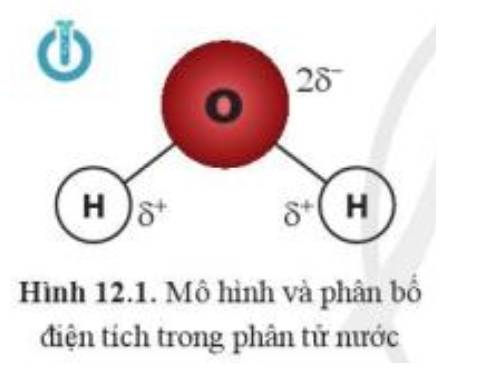
Dựa vào sự phân bố điện tích trong phân tử nước (hình 12.1), liên kết giữa hai phân tử nước được hình thành qua cặp nguyên tử O với H.
Do nguyên tử H mang điện tích dương nên liên kết với nguyên tử mang điện tích âm là O. Ngoài ra O còn 2 cặp electron riêng và độ âm điện lớn hơn H. Vì vậy phân tử H2O được tạo bởi các liên kết hydrogen của cặp nguyên tử O – H, liên kết này có bản chất tĩnh điện, tương tác hút điện giữa và , giúp liên kết hai phân tử H2O với nhau.

Chọn đáp án D
Số electron hóa trị của n nguyên tử C bằng 4n.
Giữa n nguyên tử C hình thành liên kết bằng electron hóa trị.
Số electron hóa trị còn lại bằng sẽ dùng 2 electron tạo liên kết đôi.
C=O, 2 electron tạo hai liên kết đơn C-O, còn lại 2n electron để tạo liên kết C-H.
Công thức phân tử tổng quát của este no, đơn chức là .

C. thành phần phân tử và trật tự liên kết giữa các nguyên tử trong phân tử.

Nguyên tử K liên kết với nguyên tử Cl tạo thành phân tử potassium chloride. Khi phân tử potassium chloride tan trong nước tạo thành dung dịch có t/c nào dưới đây?
A. Dẫn điện
B. Không dẫn điện
C. Dễ bay hơi
D. Dễ cháy
- Là chất rắn ở điều kiện thường.
- Thường có nhiệt độ nóng chảy và nhiệt độ sôi cao.
- Khi tan trong nước tạo ra dung dịch dẫn được điện.

Vì mỗi nguyên tử N đều có 5 electron ở lớp vỏ ngoài cùng => Cần nhận thêm 3 electron vào lớp vỏ ngoài cùng để có lớp vỏ electron bền vững tương tự khí hiếm
=> Khi 2 nguyên tử N liên kết với nhau, mỗi nguyên tử sẽ góp 3 electron ở tạo ra 3 đôi electron dùng chung

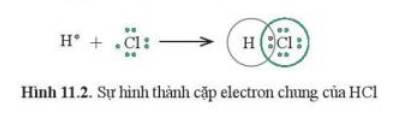

Nguyên tử H, với cấu hình electron là 1 s 1 có 1 electron hoá trị. Trong phân tử H 2 hai nguyên tử H liên kết với nhau bằng cách mỗi nguyên tử H góp 1 electron tạo thành một cặp electron chung :
Như vậy, trong phân tử H 2 mỗi nguyên tử có 2 electron giống lớp vỏ bền vững của khí hiếm heli (He).
Nguyên tử clo (Cl) có 7 electron hoá trị. Một cách tương tự, trong phân tử Cl 2 mỗi nguyên tử C1 đạt được cấu hình 8 electron ở lớp ngoài cùng giống nguyên tử khí hiếm Ar khi mỗi nguyên tử góp 1 electron tạo thành cặp electron chung :
Liên kết giữa hai nguyên tử H hay giữa hai nguyên tử C1 được gọi là liên kết cộng hoá trị.