Biết 1 mol khí etilen khi cháy hoàn toàn toả ra một nhiệt lượng là 1423 kJ, còn 1 mol khí axetilen khi cháy toả ra 1320 kJ. Hãy tính nhiột lượng toả ra khi đốt cháy 1 kg etilen, 1 kg axetilen.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Số mol của axetilen là :
11,2/22,4 x 20/100 = 0,1 mol
Số mol của etilen là :
11,2/22,4 x 80/100 = 0,4 mol
Vậy nhiệt lượng toả ra khi đốt là
(0,1 x 1320) + (0,4 x 1423) = 701,2 (kJ).

1 mol etilen tạo ra 1423kJ
0,2 mol etilen tạo ra 0 , 2 . 1423 1 = 284 , 6 K J
Đáp án: D

1. Trong 1000 m 3 khí thiên nhiên có 850 m 3 C H 4
2 C H 4 → 1500 ° C C 2 H 2 + 3 H 2
CH ≡ CH + HCl → 150 - 200 ° C , H g C l 2 C H 2 = C H - C l
Khối lượng vinyl clorua thu được (nếu hiệu suất các quá trình là 100%) là:
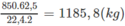
Với hiệu suất cho ở đầu bài, khối lượng vinyl clorua là:
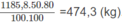
2. Nhiệt lượng cần dùng để làm nóng 100 lít nước từ 20 ° C lên 100 ° C :
100.4,18.(100 - 20) = 33440 (kJ)
Vì 20% nhiệt lượng đã toả ra môi trường nên nhiệt lượng mà khí thiên nhiên cần cung cấp phải là :
Đặt số mol C 2 H 6 tà x thì số mol C H 4 là 85. 10 - 1 x.
Ta có 1560x + 88085. 10 - 1 x = 41800
x = 462. 10 - 2
Thể tích khí thiên nhiên cần dùng:
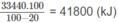


mC2H2 thực tế=1,4.1000=1400g
=>nC2H2=1400/26=700/13 mol
Mà đốt cháy 1 mol C2H2 nhiệt tỏa ra=432kJ
=>đốt cháy 700/13 mol C2H2 => nhiệt tỏa ra=23261,54kJ

\(n_{CH_4} = \dfrac{11,2.90\%}{22,4}= 0,45\ mol\)
Nhiệt lượng tỏa ra :
\(Q = 783.0,45 = 325,35\ KJ/mol\)
Thể tính khí metan CH4 = 11,2.90% = 10,08 lít
=> nCH4 = \(\dfrac{10,08}{22,4}\) = 0,45 mol
1 mol metan khi cháy tỏa ra nhiệt lượng là 783 kj
=> Khi đốt cháy 0,45 mol metan hay 11,2 lít khí bioga thì nhiệt lượng tỏa ra = 783.0,45= 352,35 kj

n C 6 H 12 O 6 = 50/180 ≈ 0,278 mol
Cứ 0,278 mol glucozơ khi oxi hóa hoàn toàn thì tỏa ra 146,3kJ
Vậy 1 mol → x? kJ
x = 146,3/0278 = 526,3kJ


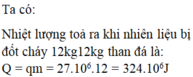

Nhiệt lượng toả ra khi đốt cháy hoàn toàn 1 kg etilen là :
1423/28 x 1000g = 50821,4kJ
Nhiệt lượng toả ra khi đốt cháy hoàn toàn 1 kg axetilen là :
1320/26 x 10006 = 50769,2kJ