Hòa tan hết hỗn hợp hai kim loại Al,Fe trong dung dịch HCl dư thấy khối lượng dung dịch thu được tăng 10,2g so với ban đầu. Cô cạn dung dịch sau phản ứng thu được 39,4g muối khan. Tính khối lượng của mỗi kim loại trong hỗn hợp đầu.
Mọi người làm dùm với ạ, đang gấp T.T


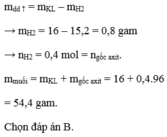
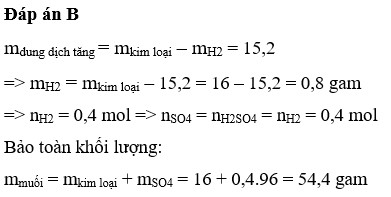
Khối lượng dung dịch tăng = m hỗn hợp kim loại - m khí H2 thoát ra
\(\Rightarrow\Delta m=m_{hh\left(kl\right)}-m_{H2}\)
\(\Rightarrow10,2=m_{hh\left(kl\right)}-m_{H2}\rightarrow m_{hh\left(kl\right)}=10,2+m_{H2}\)
Bảo toàn mol H \(\Rightarrow n_{HCl}=2n_{H2}\)
Áp dụng BTKL:
\(m_{hh\left(kl\right)}+36,5.n_{HCl}=39,4+2.n_{H2}\)
\(\Rightarrow10,2+m_{H2}+36,5.2.n_{H2}=39,4+2.n_{H2}\)
\(\Rightarrow10,2+2.n_{H2}+36,5.2.n_{H2}=39,4+2.n_{H2}\)
\(\Rightarrow n_{H2}=0,4\left(mol\right)\)
\(\Rightarrow m_{H2}=0,4.2=0,8\left(mol\right)\)
\(m_{hh\left(kl\right)}=10,2+0,8=11\left(g\right)\)
Gọi số mol Al, Fe lần lượt là x;y
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có HPT:
\(\left\{{}\begin{matrix}27x+56y=11\\1,5x+y=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Al}=0,2.27=5,4\left(g\right)\)
\(\Rightarrow\%m_{Al}=\frac{5,4}{11}.100\%=49,1\%\)
\(\Rightarrow\%m_{Fe}=100\%-49,1\%=50,9\%\)