Để trung hòa 56 gam dung dịch KOH 35% thì cần bao nhiêu ml dung dịch H2SO4 0,5M? Tính khối lượng muối thu được sau phản ứng?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

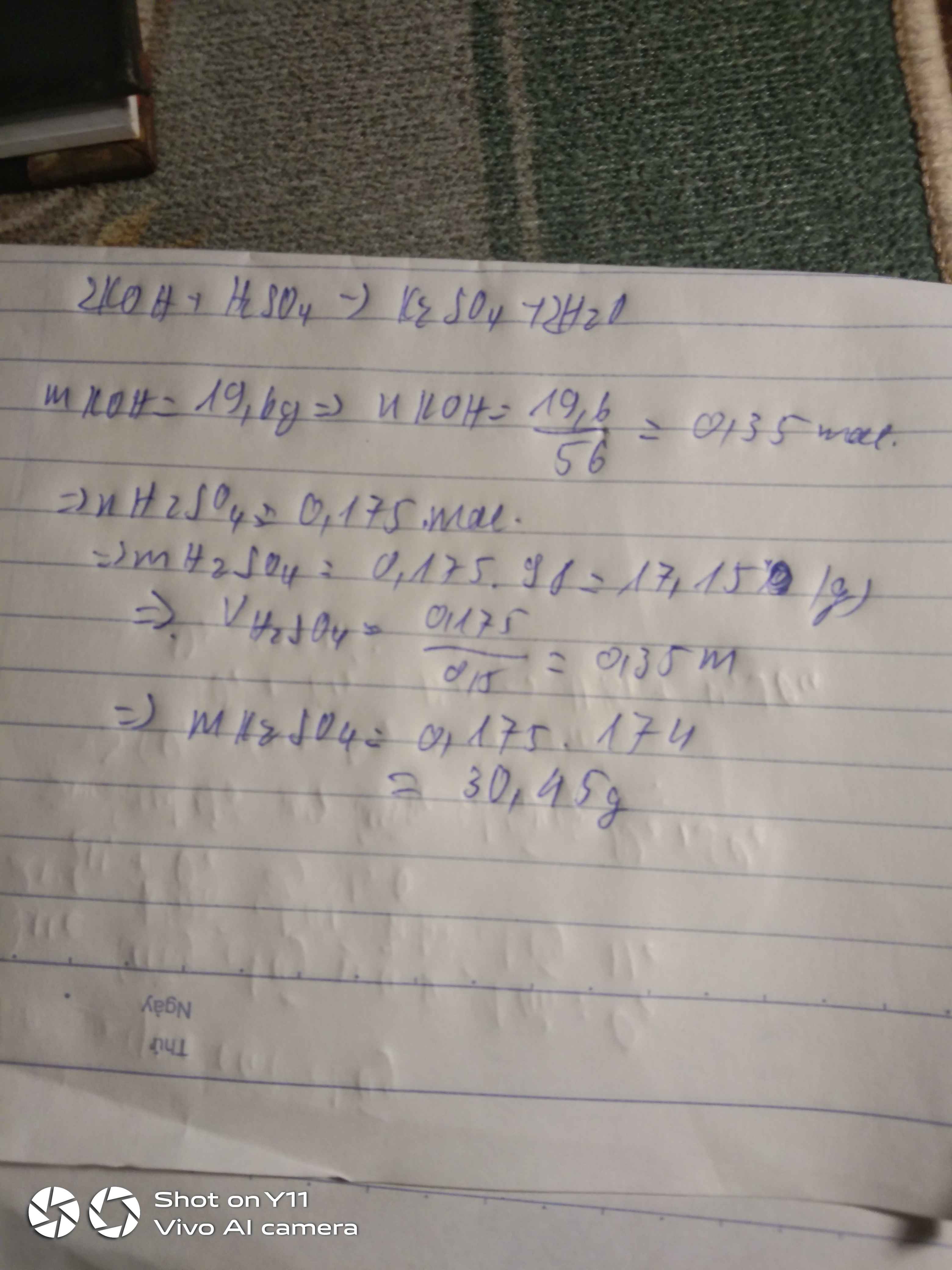

\(\text{1)}m_{KOH}=40.35\%=14\left(g\right)\\ \rightarrow n_{KOH}=\dfrac{14}{56}=0,25\left(mol\right)\\ PTHH:KOH+HCl\rightarrow KCl+H_2O\\ \text{Theo pthh}:n_{HCl}=n_{KOH}=0,25\left(mol\right)\\ \rightarrow V_{ddHCl}=0,25.0,5=0,125\left(l\right)\)
\(\text{2)}n_{Al}=\dfrac{4,05}{27}=0,15\left(mol\right)\\ n_{H_2SO_4}=200.14,7\%=29,4\left(g\right)\\ \rightarrow n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\\ \text{PTHH}:2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\\ \text{LTL}:\dfrac{0,15}{2}< \dfrac{0,3}{3}\rightarrow H_2SO_4\text{ dư}\)
\(\text{Theo pthh}:\left\{{}\begin{matrix}n_{H_2SO_4\left(pư\right)}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}.0,15=0,225\left(mol\right)\\n_{H_2}=n_{H_2SO_4\left(pư\right)}=0,225\left(mol\right)\\n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{2}.0,15=0,075\left(mol\right)\end{matrix}\right.\\ \rightarrow m_{dd\left(\text{sau phản ứng}\right)}=200+4,05-0,3.2=203,45\left(g\right)\)
\(\rightarrow\left\{{}\begin{matrix}C\%_{H_2SO_4\text{ dư}}=\dfrac{\left(0,3-0,225\right).98}{203,45}=3,61\%\\C\%_{Al_2\left(SO_4\right)_3}=\dfrac{342.0,075}{203,45}=12,61\%\end{matrix}\right.\)

\(n_{H_2SO_4}=1.0,2=0,2(mol)\\ PTHH:2NaOH+H_2SO_4\to Na_2SO_4+2H_2O\\ a,n_{NaOH}=0,4(mol);n_{Na_2SO_4}=0,2(mol)\\ \Rightarrow \begin{cases} m_{Na_2SO_4}=0,2.142=28,4(g)\\ m_{dd_{NaOH}}=\dfrac{0,4.40}{20\%}=80(g) \end{cases}\\ b,2KOH+H_2SO_4\to K_2SO_4+2H_2O\\ \Rightarrow n_{KOH}=0,4(mol)\\ \Rightarrow m_{dd_{KOH}}=\dfrac{0,4.56}{5,6\%}=400(g)\\ \Rightarrow V_{dd_{KOH}}=\dfrac{400}{1,045}=382,78(ml)\)
Bước 1: nH2SO4 = VH2SO4 . CM H2SO4= 0,2 . 1 = 0,2mol
Bước 2:
PTHH: 2NaOH + H2SO4 → Na2SO4 + H2O
2 mol 1 mol
? mol 0,2mol
nNaOH=0,2.21=0,4mol.nNaOH=0,2.21=0,4mol.
m NaOH= n NaOH.MNaOH = 0,4 . (23 + 16 + 1) = 16g
Bước 3: C% = mNaOH : m dd NaOH => mdd NaOH = mNaOH : C% = 16 : 20% = 80g

mKOH = mdd .35% = 19,6 (g)
⇒ nKOH = \(\frac{19,6}{56}=0,35\left(mol\right)\)
KOH + HCl → KCl + H2O
0,35 0,35 0,35
\(V_{HCl}=\frac{n}{C_M}=0,7\left(l\right)=700\left(ml\right)\)
mKCl = 0,35.74,5 = 26,075(mol)

Đổi 300ml = 0,3 lít
Ta có: \(n_{H_2SO_4}=0,3.0,5=0,15\left(mol\right)\)
PTHH: H2SO4 + 2KOH ---> K2SO4 + 2H2O
a. Theo PT: \(n_{KOH}=2.n_{H_2SO_4}=2.0,15=0,3\left(mol\right)\)
\(\Rightarrow V_{dd_{KOH}}=\dfrac{0,3}{0,2}=1,5\left(lít\right)\)
b. Theo PT: \(n_{K_2SO_4}=n_{H_2SO_4}=0,15\left(mol\right)\)
\(\Rightarrow m_{K_2SO_4}=0,15.174=26,1\left(g\right)\)
c. Ta có: \(V_{dd_{K_2SO_4}}=V_{dd_{H_2SO_4}}=0,3\left(lít\right)\)
\(\Rightarrow C_{M_{K_2SO_4}}=\dfrac{0,15}{0,3}=0,5M\)

Bài 1:
Ta có: \(n_{HCl}=0,2.0,5=0,1\left(mol\right)\)
BTNT H, có: \(n_{HCl}=2n_{H_2O}\Rightarrow n_{H_2O}=0,05\left(mol\right)\)
Theo ĐL BTKL, có: m oxit + mHCl = mmuối + mH2O
⇒ mmuối = 2,8 + 0,1.36,5 - 0,05.18 = 5,55 (g)
Bài 2:
\(m_{KOH}=200.5,6\%=11,2\left(g\right)\Rightarrow n_{KOH}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(2KOH+CuCl_2\rightarrow2KCl+Cu\left(OH\right)_2\)
Theo PT: \(n_{Cu\left(OH\right)_2}=\dfrac{1}{2}n_{KOH}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cu\left(OH\right)_2}=0,1.98=9,8\left(g\right)\)

100ml = 0,1l
\(n_{H2SO4}=3.0,1=0,3\left(mol\right)\)
a) Pt : \(H_2SO_4+2KOH\rightarrow K_2SO_4+2H_2O|\)
1 2 1 2
0,3 0,6 0,3
b) \(n_{K2SO4}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
⇒ \(m_{K2SO4}=0,3.174=52,2\left(g\right)\)
c) \(n_{KOH}=\dfrac{0,3.2}{1}=0,6\left(mol\right)\)
\(V_{ddKOH}=\dfrac{0,6}{2}=0,3\left(l\right)\)
d) \(V_{ddspu}=0,1+0,3=0,4\left(l\right)\)
\(C_{M_{K2SO4}}=\dfrac{0,3}{0,4}=0,75\left(M\right)\)
Chúc bạn học tốt

\(a,PTHH:KOH+HNO_3\rightarrow KNO_3+H_2O\\ b,n_{HNO_3}=3\cdot0,15=0,45\left(mol\right)\\ \Rightarrow n_{KOH}=n_{HNO_3}=0,45\left(mol\right)\\ \Rightarrow m_{CT_{KOH}}=0,45\cdot56=25,2\left(g\right)\\ \Rightarrow m_{dd_{KOH}}=\dfrac{25,2\cdot100\%}{25\%}=100,8\left(g\right)\\ c,V_{dd_{KOH}}=\dfrac{m_{dd_{KOH}}}{D}=\dfrac{100,8}{2,12}\approx47,5\left(ml\right)\)

Ta có nNaOH = 0,006 mol ; nH2SO4 = 0,028 mol
=>nH2SO4 phản ứng X = 0,05 mol = nX
=>các amino axit trong X chỉ chứa 1 nhóm NH2.
+/ Xét ½ X có số mol 0,025 . nBa(OH)2 = 0,015 mol
=>Lượng OH- trung hòa ½ X là 0,03 mol > 0,025
=>Trong X có 1 amino axit có 1 nhóm COOH ; axit còn lại có 2 nhóm COOH
=> naa có 2 nhóm COOH = 0,005 mol ; naa có 1 nhóm COOH = 0,02 mol
Đặt CT 2 amino axit là R1(NH2)(COOH) ; R2(NH2)(COOH)2
=>Tạo muối với Ba(OH)2 và nH2O = nOH- = 0,03 mol
Bảo toàn Khối lượng : m1/2 X= 2,235g
=> 0,02.( R1 + 61) + 0,005.(R2 + 106) = 2,235
=> 4R1 + R2 = 97
=>R1 = 14 (CH2) và R2 = 41 ( C3H5) TM
=> Do MB > MA => B là NH2-C3H5-(COOH)2
=>%mM(X) = 32,89%
=>D
