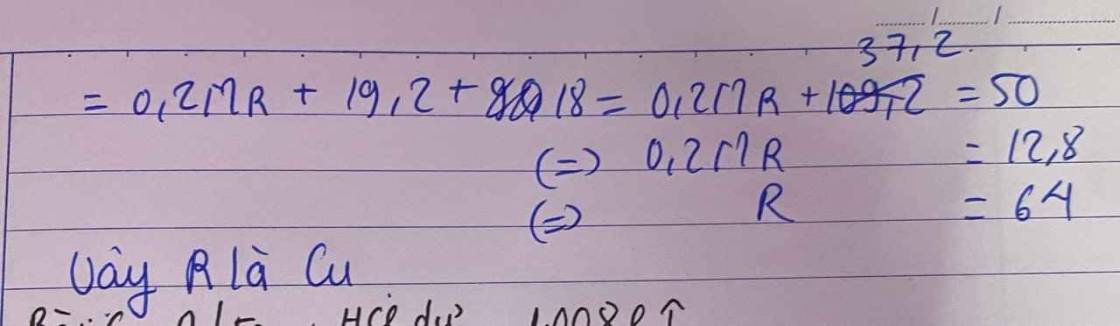đốt cháy hoàn toàn 12g muối sunfua kim loại R(R có hóa trị II không đổi ) thu được chất rắn A và khí B. hòa tan A bằng 1 lượng vừa đủ dd h2so4 14,5% thu được dd muối có nồng độ 33.33% . khi làm lạnh dd muối xuống nhiệt độ thấp hơn thì có 1 lượng tinh thể muối ngậm nước tách ra có khối lượng là 15,625 g. phần dd bảo hòa có nồng độ là 22,54% . xác định R và công thức của muối ngậm nước nói trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(2RS+3O_2\underrightarrow{^{^{t^0}}}2RO+2SO_2\)
\(RO+H_2SO_4\rightarrow RSO_4+H_2O\)
Giả sử :
\(n_{H_2SO_4}=1\left(mol\right)\)
\(\Rightarrow m_{dd_{H_2SO_4}}=\dfrac{98}{24.5\%}=400\left(g\right)\)
\(m_{\text{dung dịch muối}}=R+16+400=R+416\left(g\right)\)
\(C\%_{RSO_4}=\dfrac{R+96}{R+416}\cdot100\%=33.33\%\)
\(\Rightarrow R=64\)
\(R:Cu\)
\(n_{CuS}=\dfrac{12}{96}=0.125\left(mol\right)\)
\(n_{CuSO_4}=n_{CuS}=0.125\left(mol\right)\)
\(m_{CuSO_4}=0.125\cdot160=20\left(g\right)\)
\(m_{dd}=0.125\cdot80+\dfrac{0.125\cdot98}{24.5\%}=60\left(g\right)\)
Khối lượng dung dịch bão hòa còn lại :
\(60-15.625=44.375\left(g\right)\)
\(CT:CuSO_4\cdot nH_2O\)
\(m_{CuSO_4}=m\left(g\right)\)
\(C\%=\dfrac{m}{44.375}\cdot100\%=22.54\%\)
\(\Rightarrow m=10\)
\(m_{CuSO_4\left(tt\right)}=20-10=10\left(g\right)\)
\(\dfrac{10}{15.625}=\dfrac{160}{M_{tt}}\)
\(\Rightarrow M_{tt}=250\)
\(\Rightarrow n=5\)
\(CT:CuSO_4\cdot5H_2O\)

\(n_{CO2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : \(MCO_3+H_2SO_4\rightarrow MgSO_4+CO_2+H_2O|\)
1 1 1 1 1
0,1 0,1 0,1 0,1
\(n_{MCO3}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Có : \(0,1.\left(M=60\right)=8,4\)
\(\left(M+60\right)=84\)
\(M=84-60=24\left(dvc\right)\)
Vậy kim loại M là magie
\(n_{H2SO4}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{H2SO4}=0,1.98=9,8\left(g\right)\)
\(m_{ddH2SO4}=\dfrac{9,8.100}{12,25}=80\left(g\right)\)
\(n_{MgSO4}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{MgSO4}=0,1.120=12\left(g\right)\)
\(m_{ddspu}=8,4+80=88,4\left(g\right)\)
\(C_{MgSO4}=\dfrac{12.100}{88,4}=13,57\)0/0
Chúc bạn học tốt
Mình xin lỗi bạn nhé , bạn bố sung số mol của MgSO4 lên phương trình giúp mình và sửa giúp mình :
Pt : \(MCO_3+H_2SO_4\rightarrow MSO_4+CO_2+H_2O|\)

Gọi x là hóa trị của kim loại
Gỉa sử kim loại tham gia 1 mol => Ta có PTHH:
2R + xH2SO4 ---------> A2(SO4)x + xH2
1.........x\2.....................1\2.............x\2 (mol)
Ta có : mA = 1 . MA = A(g) ; mH2SO4= \(\frac{98x}{2}\) (g)
=> mddH2SO4 =\(\frac{\frac{98x}{2}.100}{9.8}\) = 500x (g)
=> mdd sau phản ứng = mH2SO4 + mA - mH2 = 500x + A - x (g)
=> mmuối sunfat= \(\frac{2A+96x}{2}\)(g)
Vậy nồng độ muối sau phản ứng là \(\frac{\frac{2A+96x}{2}}{500x+A-x}=\frac{15.14}{100}\)
=> A = \(\frac{2754.86}{84.86}\) x
Xét x = 1 thì A là 32.46358708 [ A là Lưu huỳnh (loại)]
x = 2 thì A là 64.92717417 [A là Zn ( nhận)]
x = 3 thì A là 97.39076125 (loại)
Vậy kim loại tham gia phản ứng là Kẽm (Zn)

a)
Fe +2 HCl --> FeCl2+ H2
R + 2HCl --> RCl2 + H2
nhh = nH2= 0,672/22,3=0,03 mol
=> M trung bình =1,52/ 0,03= 50,6
Vì MFe=56> Mtb => R<50,6
nH2SO4= 49.8%/98= 0,04 mol
R + H2SO4 --> RSO4 +H2
axit dư => nR phản ứng = nH2SO4 phản ứng <0,04
=> R>1,52/0,04= 38
Suy ra 38< R< 50,6, R hóa trị II
Vậy R là Canxi (Ca) . R =40
b)
Có nFe +nCa= 0,03mol
m hh=56nFe +40nCa =1,52
=> n Fe = 0,02 mol ; n Ca = 0,01 mol
=> %mFe, %mCa
c)
nHCl = 2nH2 =0,06 mol
=> mddHCl =36,5.0,06.100/15=14,6g
mddB= m hhkl + m ddHCl - mH2 = 1,52+ 14,6 -0,03.2= 16,06 g
dd B có FeCl2 0,02 mol và CaCl2 0,01 mol
=> C%.

Hòa tan 1,52g hh Fe và kim loại R có hóa trị II trong dd HCl 15% vừa đủ thu được 0,672lit khí (đktc) và dd B. Nếu hòa tan 1,52g kim loại R trong 49g dd H2SO4 8% thì lượng axit còn dư
a) xác định kl A
==========
Fe +2 HCl --> FeCl2+ H2
R + 2HCl --> RCl2 + H2
nhh = nH2= 0,672/22,3=0,03 mol
=> M trung bình =1,52/ 0,03= 50,6
Vì MFe=56> Mtb => R<50,6
nH2SO4= 49.8%/98= 0,04 mol
R + H2SO4 --> RSO4 +H2
axit dư => nR phản ứng = nH2SO4 phản ứng <0,04
=> R>1,52/0,04= 38
Suy ra 38< R< 50,6, R hóa trị II
Vậy R là Canxi (Ca) . R =40
Có nFe +nCa= 0,03mol
m hh=56nFe +40nCa =1,52
=> n Fe = 0,02 mol ; n Ca = 0,01 mol
=> %mFe, %mCa
c) tính nồng độ phần trăm của các chất trong dd B
nHCl = 2nH2 =0,06 mol
=> mddHCl =36,5.0,06.100/15=14,6g
mddB= m hhkl + m ddHCl - mH2 = 1,52+ 14,6 -0,03.2= 16,06 g
dd B có FeCl2 0,02 mol và CaCl2 0,01 mol
=> C%=bạn tự làm nha