Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Phần trăm nguyên tử 63Cu trong tự nhiên là: %63Cu = 100 - 27 = 73%.
Khối lượng nguyên tử trung bình của Cu là:
MCu = 65 x 0,27 + 63 x 0,73 = 63,54
Phần trăm của 63Cu trong CuSO4.5H2O là
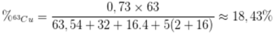

Đồng vị \(^{65}Cu\) chiếm 27% về số nguyên tử.
\(\Rightarrow\)Đồng vị \(^{63}Cu\) chiếm 73% về số nguyên tử.
Số nguyên tử khối:
\(\overline{A_{Cu}}=\dfrac{65\cdot27+63\cdot73}{100}=63,54\)
\(\%m_{^{63}Cu}=\dfrac{63\cdot0,73}{63,54+2\cdot35,5}\cdot100\%=34,18\%\)

Đáp án C
Giả sử % của 63Cu và 65Cu trong tự nhiên lần lượt là x, y
Ta có hpt:
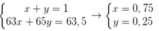
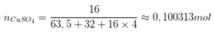
Số nguyên tử Cu = số phân tử CuSO4 = 0,100313 x 6,02 x 1023 = 6,03887 x 1022.
→ Số nguyên tử 65Cu có trong 16 gam CuSO4 là 0,25 x 6,03887 x 1022 = 1,50972 x 1022

Đáp án C.
Ta có, gọi % của đồng vị 63Cu = x, thì % đồng vị 65Cu = 100 - x
![]()
=> x = 27,3
%65Cu = 72,7%.
Đáp án C
Nguyên tử khối trung bình của đồng là MCu = 65 . 81 + 63 . 219 81 + 219 = 63,54
Trong 19,062 gam Cu có số mol là
nCu = 19 , 062 63 , 54 = 0,3 mol
→ nNO = 2 nCu : 3= 0,2 mol → V = 4,48 lít