Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Áp dụng định luật bảo toàn khối lượng ta có :
m c.rắn = mAl + m Fe2O3 = 8,1 + 48 = 56,1 g

Đáp án B
m = m Al + m Fe 2 O 3 = 8 , 1 + 48 = 56 , 1 ( gam )

Đáp án A
Ta có : nAl = 10,8 / 27 = 0,4 mol ;
nFe3O4 = 34,8 / 232 = 0,15 mol ; n H2 = 10,752 / 22,4 = 0,48 mol
8 Al + 3 Fe3O4 → 4Al2O3 + 9 Fe
8x/3 x 3x
Gọi số mol Fe3O4 phản ứng là x mol
Vì hiệu suất không đạt 100% nên cả Al và Fe3O4 đều chưa phản ứng hết.
⇒ hỗn hợp chất rắn Al dư, Fe3O4 dư , Al2O3 và Fe.
Theo phản ứng :
n Alp/ư = 8x/3 mol ⇒ nAldư = (0,4 - 8x/3) mol
2 Al + 3 H2SO4 → Al2(SO4)3 + 3H2
(0,4 - 8 3 x ) 3 2 0 , 4 - 8 3 x
Fe + H2SO4 → FeSO4 + H2
3x 3x
⇒ 3/2(0,4 - 8x/3) + 3x = 0,48 ⇒ x = 0,12 mol
⇒ H = 0,12/0,15 . 100% = 80%

Đáp án A
n Al dư = 2nH2 / 3 = 0,1 mol
⇒ H = (0,25 – 0,1)/0,25 .100%= 60%
2Al + Fe2O3 → Al2O3 +2Fe
0,15
⇒ mZ = 160.(0,15 – 0,075) + 56.0,15 = 20,4 g

Giải thích:
nAl = 0,4 mol ; nFe3O4 = 0,15 mol
Giả sử H = x
![]()
Bd: 0,4 0,15
Pu: 0,4x 0,15x 0,2x 0,45x
Sau: 0,4 – 0,4x 0,45x
nH2 = 1,5nAl + nFe → 0,48 = 1,5(0,4 – 0,4x) + 0,45x
→ x = 0,8
→ H = 80%
Đáp án D
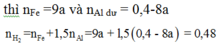
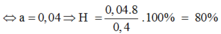
Đáp án B
Áp dụng định luật bảo toàn khối lượng ta có:
mc.rắn = mAl + mFe2O3 = 8,1 + 48 = 56,1 g