Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{AgNO3}=0,5.0,3=0,15\left(mol\right)\)
\(n_{KCl}=0,2.0,1=0,02\left(mol\right)\)
\(n_{CuCL2}=0,2.0,1=0,02\left(mol\right)\)
\(PTH:AgNO_3+KCl\rightarrow AgCl+KNO_3\)
______ 0,02________0,02__0,02____________
Tỉ lệ :\(\frac{0,15}{1}>\frac{0,02}{1}\)
Nên KCl hết, AgNO3 dư, pt tính theo số mol KCl
\(\Rightarrow m_{AgCl}=0,02.\left(108+35,5\right)=2,87\left(g\right)\)
\(\Rightarrow n_{AgNO3+dư}=0,15-0,02=0,13\left(mol\right)\)
\(PTHH:2AgNO_3+CuCl_2\rightarrow2AgCl+Cu\left(NO_3\right)_2\)
______0,04 _________0,02_____ 0,04______________
Tỉ lệ :\(\frac{0,13}{2}>\frac{0,02}{1}\)
Nên AgNO3 còn dư, CuCl2 phản ứng hết, pt tính theo nCuCl2
\(\Rightarrow m_{AgCl}=0,04.\left(108+35,5\right)=5,74\left(g\right)\)
\(\Rightarrow\Sigma m_{AgCl}=2,87+5,74=8,61\left(g\right)\)

\(HCl+AgNO_3\rightarrow AgCl\downarrow+HNO_3\\ NaCl+AgNO_3\rightarrow NaNO_3+AgCl\downarrow\\ n_{AgCl}=n_{Cl^-}=0,2.0,1+0,2.0,1=0,04\left(mol\right)\\ m_{kt}=m_{AgCl}=143,5.0,04=5,74\left(g\right)\\ Chọn.A\)

Chọn đáp án A
Kết tủa là AgCl.
n A g C l = n N a C l = 0,1.0,1 = 0,01 mol => m = 0,01.143,5 = 1,435 (gam)

Câu 1:
Gọi số mol NaCl, KCl là a, b (mol)
=> 58,5a + 74,5b = 6,81 (1)
\(n_{AgCl}=\dfrac{14,35}{143,5}=0,1\left(mol\right)\)
Bảo toàn Cl: a + b = 0,1 (2)
(1)(2) => a = 0,04 (mol); b = 0,06 (mol)
\(\left\{{}\begin{matrix}m_{NaCl}=0,04.58,5=2,34\left(g\right)\\m_{KCl}=0,06.74,5=4,47\left(g\right)\end{matrix}\right.\)
Câu 2:
Gọi số mol MgCl2, KCl là a, b (mol)
=> 95a + 74,5b = 3,93 (1)
25ml dd A chứa \(\left\{{}\begin{matrix}MgCl_2:0,05a\left(mol\right)\\KCl:0,05b\left(mol\right)\end{matrix}\right.\)
nAgNO3 = 0,05.0,06 = 0,003 (mol)
=> nAgCl = 0,003 (mol)
Bảo toàn Cl: 0,1a + 0,05b = 0,003 (2)
(1)(2) => a = 0,01 (mol); b = 0,04 (mol)
\(\left\{{}\begin{matrix}\%m_{MgCl_2}=\dfrac{0,01.95}{3,93}.100\%=24,173\%\\\%m_{KCl}=\dfrac{0,04.74,5}{3,93}.100\%=75,827\%\end{matrix}\right.\)


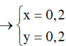
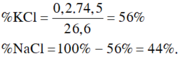
\(\Sigma CM_{hh}=0,6M\)
\(\Rightarrow n_{hh}=0,18\left(mol\right)\)
Bao toàn Cl
\(5n_{Cl\left(hh\right)}=2n_{Cl\left(kt\right)}=\frac{0,18.5}{3}=0,3\left(mol\right)\)
\(\Rightarrow m_{AgCl}=43,05\left(g\right)\)