Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cho A tác dụng với dung dịch NaOH dư lại thu được 9,85 gam kết tủa nữa =>A có Ba(HCO3)2
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
0,1<-----------0,1<---------0,1
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\)
0,05<---------0,1<--------------0,05
\(Ba\left(HCO_3\right)_2+NaOH\rightarrow BaCO_3+Na_2CO_3+H_2O\)
0,05<--------------------------------0,05
=> \(n_{Ba\left(OH\right)_2}=0,1+0,05=0,15\left(mol\right)\)
=> a =\(\dfrac{0,15}{0,5}=0,3M\)
\(n_{CO_2}=0,1+0,1=0,2\left(mol\right)\)
=>\(V_{CO_2}=0,2.22,4=4,48\left(l\right)\)

Cho A tác dụng với dung dịch NaOH dư lại thu được 9,85 gam kết tủa nữa =>A có Ba(HCO3)2
\(Ba\left(OH\right)_2+NaOH\rightarrow BaCO_3+H_2O\)
0,1<-----------0,1<---------0,1
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\)
0,05<---------0,1<--------------0,05
\(Ba\left(HCO_3\right)_{_2}+NaOH\rightarrow BaCO_3+Na_2CO_3+H_2O\)
0,05<--------------------------------0,05
=> \(n_{Ba\left(OH\right)_2}\)=0,1+0,05=0,15(mol)
=> a =0,150,5=0,3M0,150,5=0,3M
\(n_{CO_2}\)=0,1+0,1=0,2(mol)
=>\(V_{CO_2}\)=0,2.22,4=4,48(l)
từ chỗ a trở xuống , vui lòng bỏ
để mình sửa lại
\(a=\dfrac{0.15}{0.5}=0.3M\)
\(n_{CO_2}=0.1+0.1=0.2\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0.2\times22.4=4.48\left(l\right)\)

Đặt hóa trị của M là x(x>0)
\(n_{O_2}=\dfrac{4,8}{32}=0,15(mol)\\ n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ a,PTHH:4M+xO_2\xrightarrow{t^o}2M_2O_x\\ 2M+2xHCl\to 2MCl_x+xH_2\\ \Rightarrow \Sigma n_{M}=\dfrac{0,6}{x}+\dfrac{0,3}{x}=\dfrac{0,9}{x}\\ \Rightarrow M_{M}=\dfrac{8,1}{\dfrac{0,9}{x}}=9x(g/mol)\\ \text {Thay }x=3 \Rightarrow M_{M}=27(g/mol)\\ \text {Vậy M là nhôm (Al)}\)
\(b,\text {Dung dịch B là }AlCl_3\\ n_{Al}=\dfrac{8,1}{27}=0,3(mol)\\ \Rightarrow n_{AlCl_3}=n_{Al}=0,3(mol)\\ n_{Al(OH)_3}=\dfrac{15,6}{78}=0,2(mol)\\ PTHH:3NaOH+AlCl_3\to Al(OH)_3\downarrow +3NaCl\\ \text {Vì }\dfrac{n_{AlCl_3}}{1}>\dfrac{n_{Al(OH)_3}}{1} \text {nên } AlCl_3 \text { dư}\\ \Rightarrow n_{NaOH}=3n_{Al(OH)_3}=0,6(mol)\\ \Rightarrow V_{dd_{NaOH}}=0,6.2=1,2(l)\)

\(a,\) Đặt \(n_{Al}=x(mol);n_{Fe}=y(mol)\)
\(\Rightarrow 27x+56y=11(1)\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ Fe+H_2SO_4\to FeSO_4+H_2\\ Al_2(SO_4)_3+6NaOH\to 2Al(OH)_3\downarrow+3Na_2SO_4\\ FeSO_4+2NaOH\to Fe(OH)_2\downarrow+Na_2SO_4\\ \Rightarrow n_{Al(OH)_3}=x;n_{Fe(OH)_2}=y\\ \Rightarrow 78x+90y=24,6(2)\\ (1)(2)\Rightarrow \begin{cases} x=0,2(mol)\\ y=0,1(mol) \end{cases} \Rightarrow \begin{cases} m_{Al}=0,2.27=5,4(g)\\ m_{Fe}=11-5,4=5,6(g) \end{cases}\)
\(b,\Sigma n_{H_2SO_4}=1,5x+y=0,4(mol)\\ \Rightarrow V_{dd_{H_2SO_4}}=\dfrac{0,4}{0,2}=2(l)\\ c,\Sigma n_{NaOH}=3x+2y=0,8(mol)\\ \Rightarrow m_{dd_{NaOH}}=\dfrac{0,8.40}{10\%}=320(g)\\ d,2Al(OH)_3\xrightarrow{t^o}Al_2O_3+3H_2O\\ Fe(OH)_2\xrightarrow{t^o}FeO+H_2O\\ \Rightarrow n_{Al_2O_3}=0,1(mol);n_{FeO}=0,1(mol)\\ \Rightarrow m_{\text{chất rắn}}=0,1.102+0,1.72=17,4(g)\)

nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
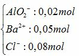 + V ml HCl 1M→ Al(OH)3: 0,01 (mol)
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)

\(a,2NaOH+MgSO_4\rightarrow Mg\left(OH\right)_2+Na_2SO_4\\ n_{NaOH}=0,5.1=0,5\left(mol\right)\\ b,n_{Mg\left(OH\right)_2}=\dfrac{0,5}{2}=0,25\left(mol\right)=n_{Na_2SO_4}\\ m_{kt}=m_{Mg\left(OH\right)_2}=58.0,25=14,5\left(g\right)\\ c,V_{ddX}=V_{ddNaOH}+V_{ddMgSO_4}=0,5+0,5=1\left(l\right)\\ C_{MddNa_2SO_4}=\dfrac{0,25}{1}=0,25\left(M\right)\)

Ta có: \(n_{HCl}=\dfrac{200}{1000}.2=0,4\left(mol\right)\)
\(PTHH:Mg+2HCl--->MgCl_2+H_2\uparrow\left(1\right)\)
a. Theo PT(1): \(n_{Mg}=n_{H_2}=n_{MgCl_2}=\dfrac{1}{2}.n_{HCl}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,2.24=4,8\left(g\right)\\V_{H_2}=0,2.22,4=4,48\left(lít\right)\end{matrix}\right.\)
b. \(PTHH:2NaOH+MgCl_2--->Mg\left(OH\right)_2\downarrow+2NaCl\left(2\right)\)
Ta có: \(n_{NaOH}=\dfrac{\dfrac{20\%.100}{100\%}}{40}=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,5}{2}>\dfrac{0,2}{1}\)
Vậy NaOH dư.
Theo PT(2): \(n_{Mg\left(OH\right)_2}=n_{MgCl_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Mg\left(OH\right)_2}=0,2.58=11,6\left(g\right)\)
a: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
200ml=0,2 lít
\(n_{HCl}=0.2\cdot22.4=4.48\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=2.24\left(mol\right)\)
\(\Leftrightarrow m_{H_2}=n_{H_2}\cdot M=2.24\cdot1=2.24\left(g\right)\)
\(n_{MgCl_2}=2.24\left(mol\right)\)
\(\Leftrightarrow n_{Mg}=2.24\left(mol\right)\)
\(\Leftrightarrow m_{Mg}=2.24\cdot24=53.76\left(g\right)\)

nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
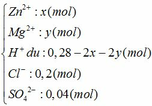
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
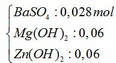
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam