Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Độ tan của muối Na 2 CO 3 ở 18 º C là: S = (53 x 100)/250 = 21,2 (gam).

\(S_{Na_2CO_3}=\dfrac{53}{250}.100=21,2\)
\(C\%=\dfrac{53}{250+53}.100\%=17,5\%\)

Ở nhiệt độ 18oC 250g nước hòa tan 53g Na2CO3 để tạo dung dịch bão hòa. Vậy ở nhiệt độ 18oC, 100g nước hòa tan Sg Na2CO3 tạo dung dịch bão hòa.
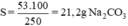
Theo định nghĩa về độ tan, ta có độ tan của Na2CO3 ở 18oC là 21,2g.

\(m_{Na_2CO_3\left(20^oC\right)}=243.\dfrac{21,5}{100+21,5}=43\left(g\right)\)
\(\Rightarrow m_{H_2O}=243-43=200\left(g\right)\)
Cứ 100g nước ở 90oC hoà tan được 43,9g Na2CO3
=> 200g nước _________________ 87,8g Na2CO3
\(\Rightarrow m_{Na_2CO_3\left(thêm.vào\right)}=87,8-43=44,8\left(g\right)\)

Gọi \(m_{Na_2CO_3}=a\left(g\right)\)
\(\rightarrow m_{H_2O}=243-a\left(g\right)\\ \rightarrow S_{Na_2CO_3\left(20^oC\right)}=\dfrac{a}{243-a},100=21,5\\ \rightarrow a=2,322\left(g\right)\)
\(\rightarrow m_{H_2O}=243-2,322=240,678\left(g\right)\)
Gọi \(m_{Na_2CO_3\left(thêm\right)}=b\left(g\right)\)
\(\rightarrow S_{Na_2CO_3\left(90^oC\right)}=\dfrac{2,322+b}{243+b}.100=43,9\\ \rightarrow b=186\left(g\right)\)

a) mdd =15+65=80g
b)
⇒SNa2CO3=\(\dfrac{53}{250}\).100=21,2g
Vậy độ tan của muối Natricacbonat ở 18 độ C là 21,2g
a. mdd = 15+65 = 80 (g)
b. Độ tan của muối Na2CO3 ở 18^oC là : S = (53 x 100)/250 = 21,2 (gam).

Ở $20^oC$ :
21,5 gam $Na_2CO_3$ hòa tan tối đa 100 gam nước tạo thành 121,5 gam dung dịch bão hòa
Suy ra :
x gam $Na_2CO_3$ hòa tan tối đa y gam nước tạo thành 243 gam dung dịch bão hòa
Suy ra : x = 43 ; y = 200 gam
Ở $90^oC$ :
$43,9$ gam $Na_2CO_3$ hòa tan tối đa 100 gam nước
Suy ra :
x gam $Na_2CO_3$ hòa tan tối đa 200 gam nước
Suy ra : x = 87,8(gam)
Suy ra : $m_{Na_2CO_3\ thêm\ vào} = 87,8 - 43 = 44,8(gam)$
S=\(\dfrac{53.100}{250}=21,2gNa2CO3\)
Theo định nghĩa về độ tan, ta có độ tan của Na2CO3 ở 18oC là 21,2g
\(S=\dfrac{53}{250}.100=21,2\left(g\right)\)